研究发现常见肠道细菌促进癌症发生
荷兰研究者Clevers等利用类器官模型,给出了感染特定的肠道细菌可导致结直肠癌突变的研究证据,研究报告在《自然》杂志提前发表。(Nature. 2020年2月27日在线版)

研究者开创性地建立了类器官的实验方法,并将其发展为研究癌症的一种重要工具。类器官是在培养皿中长出的迷你3D器官。约十年前,Clevers等首次培养出肠道类器官,将小鼠肠道中取出的干细胞放置在合适的生长环境中,经过快速繁殖和发育,长成迷你版肠道,从组织结构上重现了真正肠道的特征。之后这样的器官替身成为很多研究者研究发育和疾病的模型。类器官技术在2017年被Nature Methods评为生命科学领域年度技术。
该研究中,研究者用模拟人类肠道的类器官来研究结直肠癌是如何发生的。结直肠癌的发生与一些关键的基因突变有关,找出促进基因突变的风险因素,可以为筛查和预防结直肠癌提供指导。
肠道内大量存在的细菌也引起研究界的关注。有些肠道细菌会损伤肠壁,促进组织发炎。比如有一类大肠杆菌的菌株,基因组中含有所谓的“pks”基因岛序列(被称为pks+大肠杆菌),会合成colibactin(一种能损伤DNA的毒素)。约20%的健康人体内都有pks+大肠杆菌。而在结直肠癌患者中,携带这种大肠杆菌的人比例更高,约占60%。
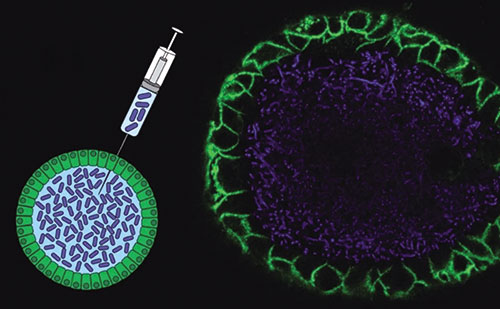
研究者计划让一些迷你肠道接触pks+大肠杆菌,让另一些迷你肠道接触pks突变、不产生毒素的大肠杆菌,从而进行对比。
经过5个月的反复注射,研究者对这些长时间接触大肠杆菌的类器官进行了全基因组测序分析,分析它们的基因特征与注射前相比有哪些改变。结果显示,相比接触不产生活性毒素的大肠杆菌,接触pks+大肠杆菌的肠道类器官出现了一些独特的基因突变特征,比如DNA单个碱基替换增多、特征性的插入缺失等。
这些基因突变特征也在真实患者的肿瘤样本中存在。研究者选取了近6000例肿瘤的全基因组测序数据。分析结果显示,前述类器官实验中发现的一些突变特征集中出现在结直肠癌来源的样本中。
研究者认为,找出这些特征对确定癌症病因有很大价值,甚至可以指导治疗策略。这些结果提示结直肠癌的突变过程可直接来源于与产生colibacin的pks+大肠杆菌的接触。基于这类细菌的常见性,有些用于治疗和临床试验的益生菌中就包含pks+大肠杆菌,研究者建议,检测和去除这类大肠杆菌菌株,并对相应的益生菌进一步研究,希望能采取相应策略降低罹患结直肠癌的风险。 (编译 姜凤琴)














