老年患癌风险下降机理研究
美国纪念斯隆-凯特琳癌症中心庄学谦等研究揭示,衰老对患癌的影响不是单一的,老年早期,肿瘤发病率升高,老年后期,衰老的基因组调控导致细胞干性下降,会抑制肿瘤的发生发展。随着个体年龄增大,体内干细胞和祖细胞等有干性的细胞数量下降、细胞肿瘤发生所需的,这些细胞数量下降降低了肿瘤发生风险。(Nature. 2024年12月4日在线版)
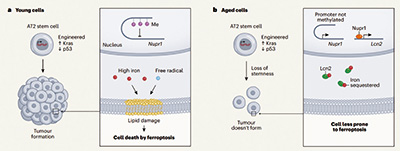
实验发现,随着年龄增长,小鼠会产生更多的Nupr1蛋白,使肺部细胞表现出缺铁的状态,失去再生能力,这种再生能力与肿瘤发生直接相关,导致老年小鼠较年轻小鼠患癌概率小很多。给老年小鼠补充额外的铁或减少细胞内Nupr1,这种效果会出现逆转。
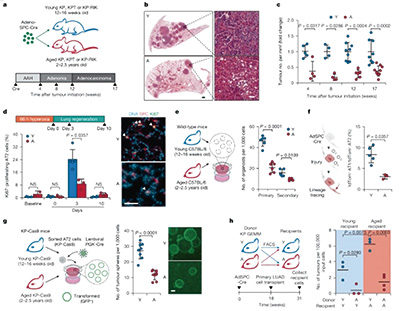
研究者选择一种基因修饰的肺腺癌小鼠模型,选取不同年龄的小鼠进行实验,分别是鼠龄12~16周的年轻小鼠和鼠龄104~130周的老年小鼠,通过特定腺病毒载体在小鼠AT2细胞中引入癌症突变,这类细胞是位于肺泡结构中的干细胞,既能帮助组织再生,也与肺腺癌发生相关。
观察结果显示,进行肿瘤激活处理后,老年小鼠中位存活期较年轻小鼠长37%,老年小鼠体内肿瘤数量较年轻小鼠少,肿瘤负荷也小,肿瘤体积小40%~60%,提示衰老或对肿瘤起始有一定的抑制作用。
研究显示,肿瘤起始对相关组织中细胞的自我更新及分化能力即干性的要求非常高。相比于年轻小鼠,老年小鼠体内AT2细胞密度减少约47%。肺部损伤实验显示,AT2细胞增殖能力、肺泡再生能力均大幅下降。从数量和质量上,AT2细胞支持肿瘤发生的可能性在年老小鼠中已降低了。
研究者发现,AT2细胞干性丢失是AT2的铁敏感度出现了问题,老年小鼠AT2细胞中,名为Nupr1的蛋白高表达,该蛋白通过激活下游特定基因调控细胞内铁水平。当Nurp1过高时,细胞对铁水平的判断出现异常,它们会认为细胞没有足够的铁,从而降低细胞的干性。在老年小鼠中抑制Nupr1,肿瘤会恢复起始和生长能力。
该研究发现对基于铁死亡的新型肿瘤治疗策略有重要意义。铁死亡疗法目前已有一些诱导铁死亡的小分子化合物及之前获批的药物在研发中,这类疗法有杀灭肿瘤细胞的潜力。该研究发现,年老细胞较年轻细胞对铁死亡的抵抗力强很多,年老个体细胞对铁感知出现异常,使得这类疗法或更适合年轻患者。
研究者指出,该研究发现支持癌症预防越早越好,年轻时吸烟、紫外线、接触致癌物质等带来的患癌风险比年老时大得多,提示年轻人群加强癌症预防尤为重要。不过有评论专家指出,年老人群发病率下降可能是统计学上的偏倚造成的。虽然癌症登记数据显示,65~84岁人群癌症高峰期后发病率有所下降,不过尸检统计数据显示,高龄老年人群癌症发病仍持续增加,提示高龄人群缺乏癌症相关诊断或是癌症发病率下降原因。肺癌的情况有所特殊,将尸检结果考虑在内,仍显示高龄人群高峰期后发病率下降,所以该研究结果能否推及其他瘤种仍未可知。不过该研究为开展衰老相关癌症防治策略提供了参考,Nupr1或可作为新的靶点,利用人体衰老机制发挥抗击肿瘤的作用或是研究方向。
(编译 张俊熙)










