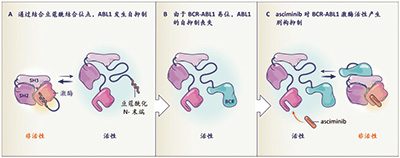
新发的、费城染色体阳性CML-CP asciminib继续保持优于最佳标准治疗的优势
美国佐治亚州癌症中心Cortes报告,在新发的、费城染色体阳性的、慢性期慢性髓细胞白血病(CML-CP)患者中,与标准的酪氨酸激酶抑制剂(TKI)相比,asciminib显示出较高的96周主要分子缓解(MMR)率,且在包括伊马替尼和第二代TKI在内的不同亚组中均有显著差异。(摘要号475)
Ⅲ期研究ASC4FIRST招募了新发的、费城染色体阳性的、没有接受过TKI治疗的、CML-CP成年患者,分予asciminib(80 mg qd)或研究者选择的标准的TKI。
在2024年10月22日数据截止时,asciminib组和标准TKI组分别有81.6%和60.3%的患者接受相应的治疗;治疗中断率分别为17.9%和38.2%,其中疗效不满意所致分别为9.5%和20.6%,不良事件所致分别为6.0%和12.7%,疾病进展所致分别为1.0%和2.0%,医生决定所致分别为0.5%和0.0%),方案偏差所致分别为0.5%和1.0%,患者决定所致分别为0.5%和1.5%,妊娠所致分别为0.0%和0.5%。
asciminib组和标准TKI组的48周MMR率分别为68%(95%CI 61%~74%)和49%(95%CI 42%~56%),率差为19%(95%CI 10%~28%,P<0.001);在伊马替尼分层队列中48周MMR率分别为69%(95%CI 59%~78%)和40%(95%CI 31%~50%),率差为30%(95%CI 17%~42%,P<0.001)。基于这些数据,2024年10月29日,FDA加速批准asciminib治疗新发的费城染色体阳性CML-CP成年患者的申请。
本次ASH年会上更新的结果显示,在第96周时,asciminib组(201例)和标准TKI组(204例)患者的MMR率分别为74.1%和52.0%,率差为22.4%(95%CI 13.6%~31.3%,P<0.001),达到该试验的一个关键次要终点,同时主要终点48周MMR率分别为67.7%和49.0%。
在伊马替尼分层队列中,asciminib组(101例)和标准TKI组(102例)的96周MMR率分别为76.2%和47.1%,率差为29.7%(95%CI 17.6%~41.8%,P<0.001)。
在第二代TKI分层队列中,asciminib组(100例)和标准TKI组(102例)的96周MMR率分别为72.0%和56.9%,率差为15.1%(95%CI 2.3%~28.0%)。
在深度分子缓解方面,第96周时,asciminib组和标准TKI组分别有48.8%和27.5%的患者达到MR4,分别有30.9%和17.7%的患者达到MR4.5。伊马替尼分层队列中asciminib治疗使52.5%的患者达到MR4,使35.6%的患者达到MR4.5;标准TKI组中这两指标则分别为23.5%和11.8%。第二代TKI分层队列中asciminib治疗使45.0%的患者达到MR4,使26.0%的患者达到MR4.5;标准TKI组中这两指标则分别为31.4%和23.5%。
第96周时,asciminib的安全性和耐受性继续优于伊马替尼和第二代TKI。在asciminib(200例)、伊马替尼(99例)和第二代TKI(102例)患者构成的安全性人群中,≥3级不良事件发生率分别为44.5%、49.5%和59.8%,导致治疗中断的不良事件发生率分别为5.0%、13.1%和12.7%,导致剂量调整/中断的不良事件发生率分别为33.0%、41.4%和57.8%。
(编译 张梓轩)










