儿童和青年淋巴瘤 纳武利尤单抗单药安全耐受
美国斯坦福大学Davis等报告,纳武利尤单抗3 mg/kg治疗儿童和青年淋巴瘤也安全耐受,但单药治疗其他常见的儿童实体瘤则没有显著的抗瘤活性。(Lancet Oncol. 2020年3月17日在线版)

针对PD-1的免疫检查点抑制剂已在成人癌症患者中显示出临床获益,但其在儿童患者中的数据很少。为了明确其对儿童和青年复发/难治性非CNS实体瘤或淋巴瘤患者的安全性、药代动力学和抗肿瘤活性,该项多中心单臂、开放标签的、剂量确证和剂量扩展的Ⅰ/Ⅱ期研究在美国23家医院入组患者。
剂量确证阶段(A部分)入组条件:1~18岁;有可测量或可评估病灶的实体瘤(RECIST 1.1版标准),任何组织学类型均可。剂量扩展阶段(B部分)入组条件:1~30岁;有可测量病灶(RECIST标准);横纹肌肉瘤,尤因肉瘤,骨肉瘤,神经母细胞瘤,霍奇金淋巴瘤,非霍奇金淋巴瘤和黑色素瘤。
在连续6轮研究设计中,A部分的给药方案为60分钟内输注纳武利尤单抗3 mg/kg d1、15 q28,并根据剂量限制毒性进行降阶梯治疗以确定推荐的Ⅱ期剂量;B部分的给药方案为推荐的Ⅱ期剂量。主要终点为儿童和青年患者在成人推荐剂量下的耐受性,全身暴露情况,最大耐受剂量和抗肿瘤活性。
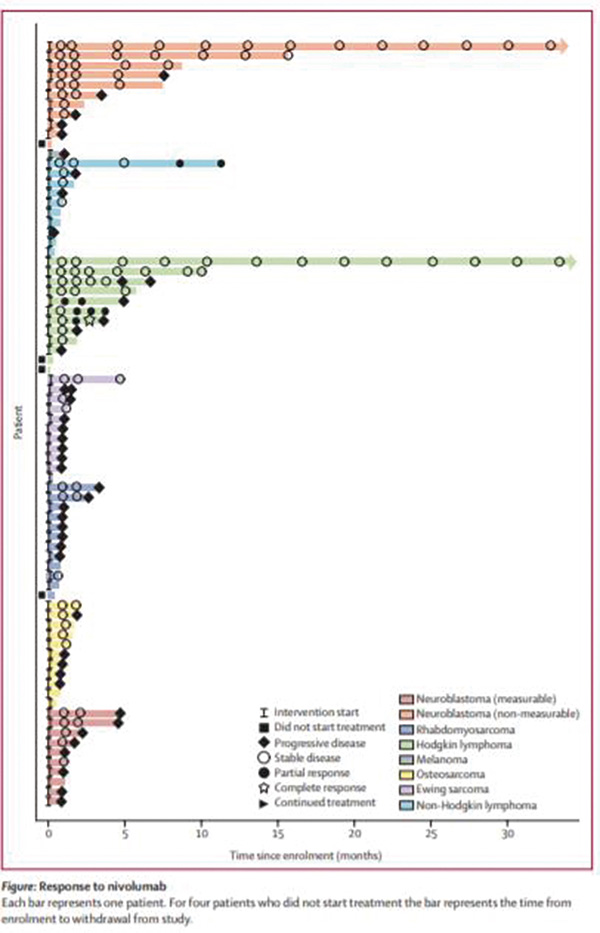
结果显示,2015年2月22日至2018年12月31日,共入组85例患者,其中75例可评估毒性。中位随访30天(IQR:27~83天)。A部分入组13例患者,其中12例可评估毒性。未见降阶梯治疗剂量或剂量限制性毒性反应,所以纳武利尤单抗儿童患者的2期推荐剂量为3 mg/kg。B部分入组72例患者,其中63例可评估毒性。B部分中有5例(7%)发生剂量限制性毒性。
最常见的毒性事件为贫血(35例,47%;其中5例为3级或4级),非血液学毒性为疲劳(28例,37%;未见3级或4级事件)。淋巴瘤患者有效,疗效见于3例(30%)霍奇金淋巴瘤患者和1例(10%)非霍奇金淋巴瘤患者,所有应答者均表达PD-L1。其他类型肿瘤无客观缓解。
(编译 田启龙)














