一线治疗较高危的MDS 联用Sabatolimab安全但未改善疗效
美国耶鲁癌症中心Zeidan等报告,去甲基化药物一线治疗较高危的骨髓增生异常综合征(MDS)患者时,联用Sabatolimab并未显著改善完全缓解率或无进展生存期(PFS),但该药在大多数患者中的安全性可控。(Lancet Haematol. 2023年12月5日在线版)
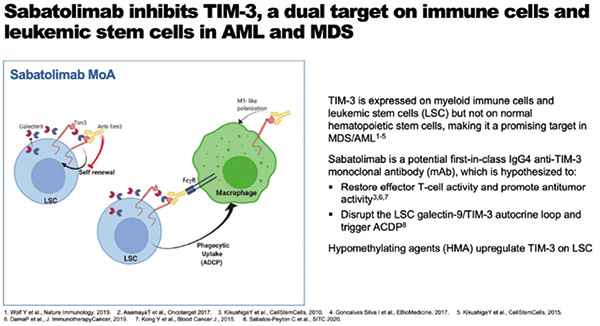
Sabatolimab是一种靶向T细胞免疫球蛋白结构域和黏蛋白结构域-3(TIM-3)的免疫疗法,而TIM-3是一种在免疫细胞和白血病干细胞上表达的免疫—髓系调节因子。
为了比较Sabatolimab联合去甲基化药物对比安慰剂联合去甲基化药物一线治疗较高危的MDS患者时的疗效和安全性,该项多中心、随机双盲、安慰剂对照Ⅱ期研究(STIMULUS-MDS1)在17个国家的54个研究站点纳入≥18岁的、未经治的、标危/高危/极高危的MDS患者,给予去甲基化药物(地西他滨20 mg/m2 d1~5 q28;或阿扎胞苷75 mg/m2 d1~7 q28,或d1~5、8、9 q28),同时随机等比分别联用Sabatolimab(400 mg d8、22)或联用安慰剂,直至治疗停止。两个主要终点为完全缓解率和PFS。
结果显示:2019年7月29日至2020年8月10日,联用Sabatolimab组和联用安慰剂组分别随机入组患者65例和62例;总体患者的中位年龄为73岁(IQR:69~77岁),其中86例(68%)为男性,77例(61%)为白人。
该研究未达到主要终点。截至2021年3月10日,联用Sabatolimab组和联用安慰剂组分别有14例(22%,95%CI 12.3%~33.5%)和11例(18%,95%CI 9.2%~29.5%,P=0.77)患者达到完全缓解。
截至2022年3月1日最终分析时,联用Sabatolimab组和联用安慰剂组关于PFS的中位随访时间分别为17.8个月(IQR:16.6~19.4个月)和19.2个月(IQR:17.7~22.3个月),中位PFS分别为11.1个月(95%CI 7.6~17.6个月)和8.5个月(95%CI 6.9~11.3个月;HR=0.75,95%CI 0.48~1.17,P=0.1022)。
最常见的、任何级别不良事件为中性粒细胞减少症(联用Sabatolimab组和联用安慰剂组:56% vs. 68%)、血小板减少症(48% vs. 51%)、便秘(47% vs. 38%)、腹泻(44% vs. 22%)、贫血(35% vs. 54%)、发热性中性粒细胞减少症(35% vs. 24%)和白细胞减少症(24% vs. 32%)。在联用Sabatolimab组,1例患者出现了严重的潜在的治疗相关免疫介导的不良事件,1例因肺炎导致治疗相关性死亡。
(编译 李佳)














