预防顺铂为主方案所致的恶心/呕吐 HR20013+DEX非劣效于FAPR+PALO+DEX
中山大学肿瘤防治张力教授报告,在预防顺铂为主的高度致吐性化疗所致的恶心/呕吐(HEC-CINV)方面,HR20013+DEX方案非劣效于FAPR+PALO+DEX方案,且耐受性良好。(摘要号OA07.05)
以顺铂为主的化疗仍然是晚期NSCLC治疗的核心方案。为了控制顺铂为主HEC-CINV,临床需要同时使用多种能抑制多个分子通路的止吐药。HR20013是一种HRS5580(新型NK-1受体抑制剂)和palonosetron(PALO)的混合制剂,静脉给药(IV)后能同时抑制NK-1和5-HT3通路。

为了评估HR20013联合地塞米松(HR20013+DEX)方案对比福沙吡坦(FAPR)联合palonosetron和地塞米松(FAPR+PALO+DEX)方案在预防顺铂为主HEC-CINV方面的疗效,该项多中心、随机、双盲、双模拟、阳性对照Ⅲ期临床试验(PROFIT研究)纳入顺铂为主HEC治疗的化疗初治患者,等比分予HR20013+DEX(373例)或FAPR+PALO+DEX(377例),并按照性别、年龄(≥55岁 vs.<55岁)、顺铂联合其他HEC药物(是 vs. 否)来分层。
主要终点是第1周期顺铂为主HEC治疗后全时段(OP:0~120小时)内的完全缓解(CR)率。
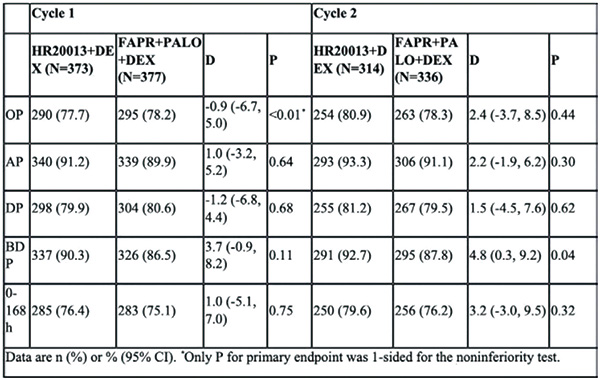
结果显示,两组的基线特征均衡。第1周期全时段内两组的CR率分别为77.7%和78.2%(P<0.01),研究达到非劣效性主要终点。
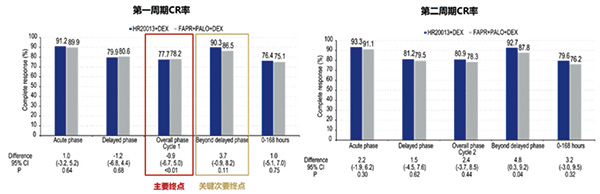
在第2周期、急性阶段(AP:0~24小时)、延迟阶段(DP:24~120小时),以及第1、2周期的0~168小时内,两组的CR率相似。
在第1、2周期的延迟后阶段(BDP:120~168小时),HR20013+DEX组的CR率高于FAPR+PALO+DEX组(第1周期:90.3% vs. 86.5%;第2周期:92.7% vs. 87.8%)。
在BDP阶段,HR20013+DEX组的完全预防作用(CP)和完全控制作用(TC)占比均较高,尤其是在第2周期(CP:90.8% vs. 86.3%;TC:83.8% vs. 78.6%)。
第1、2周期内无显著恶心、无呕吐和无额外干预的患者比例相当。两组的安全性特征相似。
HR20013是恒瑞医药自主研发的Ⅰ类新药,目前首个适应证上市申请已被CDE受理。HR20013是由Fosrolapitant(新型NK-1受体拮抗剂,218 mg)和帕洛诺司琼(5-HT3 受体拮抗剂,0.25 mg)组成的复方注射剂,是一款新型超长效止吐药物,可同时拮抗NK-1和5-HT3受体,从而发挥止吐作用。HR20013仅需每个周期用药一次,即可覆盖急性期,延迟期以及超延迟期,简化了用药管理,兼顾了安全有效性和依从性。
(编译 吴英)














