Richter转化患者 epcoritamab单药后线治疗或有抗肿瘤活性
荷兰阿姆斯特丹大学医学中心Kater等报告,在Richter转化患者中,单用CD3×CD20双特异性抗体epcoritamab可获得有临床意义的抗肿瘤活性,但总缓解率低于50%的替代性假设的阳性阈值,安全性与以往报道一致。这些发现支持进一步研究该药作为Richter转化患者的潜在治疗选择。[Lancet Haematol. 2026; 13(1): e8-e21.]
Richter转化是最难治疗的B细胞淋巴瘤之一,对携带高危慢性淋巴细胞白血病特征的患者或接受过慢性淋巴细胞白血病治疗的患者而言尤甚。多种治疗方法的中位生存期仍为6~12个月。为了评估epcoritamab单药在Richter转化患者中的安全性和初步活性,该项多中心、开放标签、Ⅰb/Ⅱ期临床试验(EPCORE CLL-1)在9个国家的24个中心纳入相关患者。入组条件:患者年龄≥18岁;患有组织学确诊的、Richter转化疾病(弥漫性大B细胞淋巴瘤DLBCL);ECOG PS评分为0~2分;接受过最多二线的、针对Richter转化的治疗。
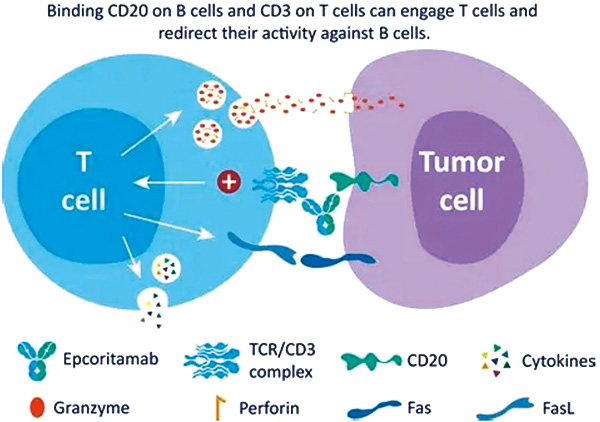
该试验包括剂量递增和剂量扩展阶段。扩展阶段评估了epcoritamab单药疗法(2A组),epcoritamab联合来那度胺(2B组),epcoritamab联合利妥昔单抗、环磷酰胺、多柔比星、长春新碱和泼尼松(R-CHOP;2C组)。主要终点为根据Lugano 2014标准在全分析集评估的总缓解率。
当前报告描述了2A组的结果。epcoritamab采用皮下注射,剂量分组增加,1~3周期每周48 mg,4~9周期每2周,之后每4周服用,直至病情进展或出现不可接受的毒性。
结果显示,2021年10月18日至2025年3月21日,研究招募了42例Richter转化患者。患者的中位年龄为69岁(50~80岁),其中32例(76%)为男性,37例(88%)为白人,2例(5%)为亚裔,1例(2%)为黑人或非洲裔美国人,2例无族裔信息。从诊断慢性淋巴细胞白血病或小淋巴细胞瘤到Richter转化的中位时间为7.6年(0~23.9年)。21例(50%)接受epcoritamab作为一线Richter转化导向治疗。
中位随访22.9个月(0.5~39.9个月)时,20例患者获得了缓解,研究者评估的总缓解率为47.6%(95%CI 32.0%~63.6%),但未达到预设的替代假说阈值(50%)。在21例一线治疗人群、21例二线及以上治疗人群和20例基线时携带TP53异常和/或del(17p)改变的人群中,总缓解情况分别有12例(总缓解率为57.1%,95%CI 34.0%~78.2%)、8例(38.1%,95%CI 18.1%~61.6%)和8例(40%,95%CI 19.1%~63.9%)。
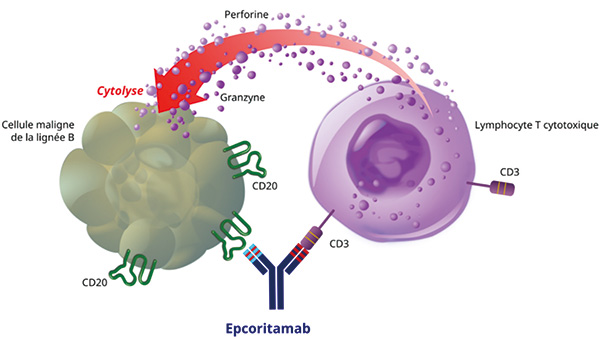
最常见的3~4级不良事件为中性粒细胞减少(19例次,45%)、贫血(16例次,38%)、血小板减少(16例次,38%)、感染(9例次,21%)、肺炎(4例次,10%)和COVID-19(2例次,5%)。细胞因子释放综合征有36例次(86%),其中3例次(7%)为3级。免疫效应细胞相关神经毒性综合征有5例次(12%,均为1~2级)。临床肿瘤溶解综合征有2例次(5%,均为1~2级)。研究报告了3例次致命性的不良事件,原因分别为导致全身健康恶化的进行性疾病、脓毒症和脑血管意外;研究者认为这些都与研究治疗无关。
有评论者表示:虽然epcoritamab在全体队列中的总缓解率未到达预设的阳性阈值,但在接受epcoritamab作为一线治疗的患者中结果令人鼓舞。这种总体的阴性结果反映了这一侵袭性疾病所面临的治疗困局;不过,随着每一种新疗法的测试,疗效正在逐步改善,为患者带来了新的希望。
(编译 魏强)


