国人研究发现前列腺癌生长机制关键非编码RNA
清华大学生命学院杨雪瑞等通过研究,明确了长非编码RNA(lncRNA)NEAT1在前列腺癌细胞中的促癌作用,首次提出NEAT1协助转录因子CDC5L调控靶基因AGRN,从而促进肿瘤细胞增殖与肿瘤生长的新机制。(Cancer Res. 2018 年6月5.日在线版 doi: 10.1158/0008-5472.CAN-18-0688)
NEAT1是一种长约3.2kb的非编码RNA,主要富集于细胞核中,是形成与维持细胞核亚结构(paraspeckle)的关键非编码RNA。在前列腺癌中,NEAT1被发现有促癌作用,但其分子机制并不清楚。杨雪瑞研究组的主要研究方向之一是lncRNA在癌症中的生理功能与分子机制。
鉴于lncRNA种类复杂、功能多样、已知信息缺乏,研究者首先采用多组学大数据挖掘手段,设计一系列数据整合分析算法,通过对细胞内转录调控关系的定量分析,鉴定影响重要转录调控通路的lncRNA分子。
研究者使用了癌症大规模组学数据库TCGA (The Cancer Genome Atlas)的资源,基于约500例前列腺癌组织的多组学数据,系统分析了该类肿瘤环境中lncRNA对转录调控网络的影响。
分析结果显示,NEAT1可能调控多个转录因子的功能活性,其中转录因子CDC5L与NEAT1有直接的互作结合。在此基础上,研究者设计了一系列分子生物学与癌症生物学实验,不仅验证了数据分析所作的预测,而且详细阐明了NEAT1在前列腺癌中促癌作用的分子机制。
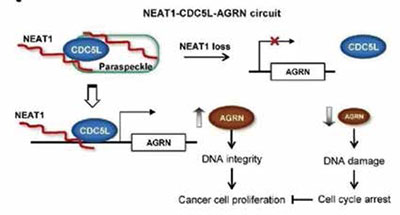
研究发现,NEAT1招募并富集CDC5L蛋白至细胞核中的paraspeckle,促进CDC5L对靶基因AGRN的转录激活作用,而在前列腺癌细胞中,AGRN起到了促进DNA损伤修复的作用。对NEAT1表达水平的敲低抑制了CDC5L-AGRN转录调控通路的活性,导致前列腺癌细胞DNA损伤的累积,从而影响了细胞周期与增殖。
许多肿瘤中有p53等DNA损伤修复机制的缺失,因此,在肿瘤细胞中诱导大规模DNA损伤有抑制肿瘤发展的功能。杨雪瑞研究组首次发现非编码RNA NEAT1在控制DNA损伤、维持肿瘤细胞增殖与细胞周期中的关键作用。基于此机制,NEAT1表现出作为前列腺癌治疗靶点的潜力。
(编译 宋茜)