cT2~T3bN0M0期肌层浸润性膀胱癌 部分患者或可选择围手术期戈沙妥珠单抗联合帕博利珠单抗

意大利IRCCS圣拉斐尔医院综合癌症中心Necchi等报告,不宜或拒绝含顺铂新辅助化疗的cT2~T3bN0M0期肌层浸润性膀胱癌患者,围手术期的戈沙妥珠单抗联合帕博利珠单抗方案显示出有前景的临床完全缓解率,未发生4级及以上不良事件,约40%的患者实现膀胱保留并获得持续缓解。(Lancet Oncol. 2026年2月27日在线版; 2026 ASCO GU大会. 摘要号769)
肌层浸润性膀胱癌的标准治疗是新辅助化疗联合根治性膀胱切除术,但约50%的患者不符合新辅助化疗的条件或拒绝接受该治疗。帕博利珠单抗和戈沙妥珠单抗单药新辅助治疗肌层浸润性膀胱癌均已显示出疗效。
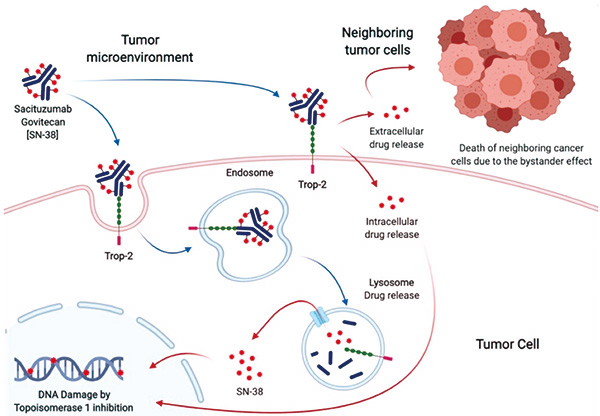
为了评估戈沙妥珠单抗联合帕博利珠单抗新辅助治疗—保留膀胱手术—帕博利珠单抗辅助治疗的临床活性,该项单臂Ⅱ期研究(SURE-02)在意大利米兰IRCCS圣拉斐尔医院进行,先予4个周期的帕博利珠单抗(200 mg d1 q21)联合戈沙妥珠单抗(7.5 mg/kg d1、8 q21)新辅助治疗,随后进行根治性膀胱切除术或经尿道膀胱肿瘤再次电切术(re-TURBT;经多学科肿瘤委员会讨论),最后给予13个周期的帕博利珠单抗(200 mg d1 q21)辅助治疗。
入组条件:患者年龄≥18岁;ECOG PS 评分为0~1分;新发的、组织学确诊的、肌层浸润性膀胱癌,分期为cT2~T3bN0M0期;被认定不符合或拒绝接受基于顺铂的新辅助化疗,并拟安排根治术治疗。
主要终点为临床完全缓解率,定义为未接受根治性膀胱切除术的患者在re-TURBT时影像学阴性且无存活肿瘤。
结果显示,2023年10月2日至2025年2月26日,研究筛查的63例患者中有49例被纳入治疗并可被评估安全性和有效性,其中位年龄为66岁(IQR:61~71岁),其中8例(16%)为女性,48例(98%)为白人,1例(2%)为黑人。33例(67%)为cT2期,21例(43%)经中央评估确诊组织学类型。
中位随访14个月(IQR:8~18个月)后,19例(39%,95%CI 25%~54%)患者获得临床完全缓解,他们都接受了re-TURBT;luminal亚型患者的临床完全缓解率高于non-luminal亚型的(57% vs. 33%,P=0.073)。所有临床完全缓解的患者均无转移,2例患者出现膀胱内复发。3级治疗相关不良事件有8例(16%),其中最常见的是腹泻(4例,8%)。研究未见治疗相关的死亡病例。3例(6%)患者报告严重的治疗相关不良事件,其中2例为大疱性类天疱疮,1例为结肠炎。
研究解读
美国马萨诸塞大学Mittal等表示:SURE-02研究为部分经选择的、仅采用了全身治疗的患者未来保留膀胱提供了路径,表明戈沙妥珠单抗联合帕博利珠单抗是一种有活性的组合,值得被进一步研究。高活性方案如抗体-药物偶联物联合免疫检查点抑制剂,无论是否符合顺铂治疗的条件,在生物标志物指导下,都有潜力减少肌层浸润性膀胱癌患者对巩固治疗的需求,并能改善总体结局,帮助重写患者的癌症历程。
总体而言,抗体-药物偶联物正在重塑新辅助治疗的标准,标志着摆脱顺铂依赖的趋势。接受抗体-药物偶联物联合免疫检查点抑制剂治疗的患者表现出显著的病理完全缓解率,促使医生们在保留膀胱模型中评估该方案。未来研究应完善反应适应的基准,识别出真正受益于联合治疗或辅助治疗的患者群体。(编译 郝羽)














