T-DXd治疗HER2低表达/不表达患者DAISY研究

会上报告了T-DXd治疗HER2低表达/不表达患者DAISY研究,该研究是一项多中心、开放标签Ⅱ期研究,旨在评估T-DXd 5.4 mg/kg治疗晚期乳腺癌(ABC)的疗效并进行广泛生物标志物分析。研究显示,T-DXd在HER2阳性ABC患者中,甚至HER2低表达和HER2不表达患者中均具有临床有意义的活性,安全性和之前报道一致。(摘要号 PD8-02)
研究包括3个队列:队列1(HER2阳性:HER2 IHC3+或HER2 IHC2+/ISH+),队列2(HER2低表达:IHC1+或IHC2+/ISH-),队列3(HER2不表达:IHC0~1+)。在基线,治疗中(队列1必须,队列2和3可选)和肿瘤进展时行转移灶活检。基线时收集循环肿瘤DNA(ctDNA)血液标本。
主要终点是每个队列的研究者评估最佳疗效(BOR)。次要终点为中心评估BOR,临床获益率(CBR),疗效持续时间(DoR),无进展生存期(PFS),总生存期(OS)和安全性。
2019年11月至2021年3月,185例女性患者和1例男性患者入组。患者中位年龄是55岁(24~82岁),都接受过至少一线治疗,27例患者为三阴性(TNBC)。中位随访15.6个月后,ITT人群的研究者确认BOR为48.6%,中位DoR为8.5个月,中位PFS为7.0个月。

队列1(HER2阳性)患者的BOR为70.6%,中位DoR为9.7个月,中位PFS为11.1个月;队列2(HER2低表达)患者的BOR为37.5%,中位DoR为7.6个月,中位PFS为6.7个月(HR+:6.9个月;TNBC:3.5个月);队列3(HER2不表达)患者的BOR为29.7%,中位DoR为6.8个月,中位PFS为4.2个月(HR+:4.5个月;TNBC:2.1个月)。
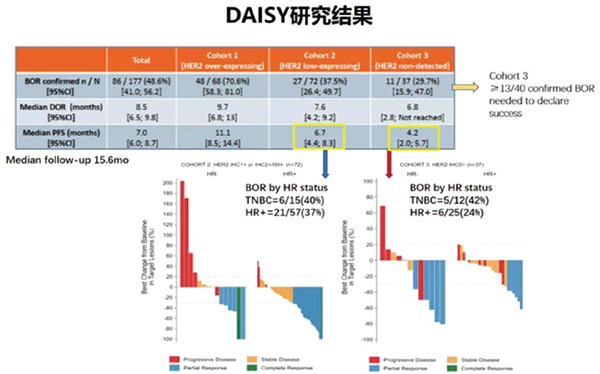
安全性方面,170例(95%)患者至少发生一种治疗相关毒性。关键≥2级治疗相关毒性包括中性粒细胞减少(10.6%),乏力(5.6%),白细胞减少(4.5%),呕吐(4.5%)和贫血(3.4%)。2.8%(5/179)患者发生药物相关性间质性肺疾病或非感染性肺炎(4例1级,1例2级),13例患者因治疗相关不良事件停药。没有药物相关死亡发生。
多项研究证实肿瘤HER2表达具有显著异质性,应重新考虑HER2表达定义标准和治疗决策依据,T-DXd在HER2低表达乃至HER2不表达肿瘤中显示出肯定的疗效,提示所有HER2低表达患者在病程中可考虑T-DXd等具有强大活性的ADC药物治疗。
(编译 胡静)














