复发转移性宫颈癌 纳武利尤单抗单药或联合伊匹单抗可行
西班牙Vall d'Hebron癌症研究所Oaknin等报告的研究显示,治疗复发或转移性宫颈癌,纳武利尤单抗单药和纳武利尤单抗联合伊匹单抗在CheckMate 358研究中显示为可行的治疗方案,未来可继续开展纳武利尤单抗联合伊匹单抗或其他双药免疫治疗方案在这类患者人群中的研究。(Lancet Oncol. 2024年4月9日在线版)
CheckMate 358研究的初步结果显示,纳武利尤单抗单药和纳武利尤单抗联合伊匹单抗在复发或转移性宫颈癌中有持久抗肿瘤反应,联合方案有临床活性。目前研究者报告了长期随访结果。
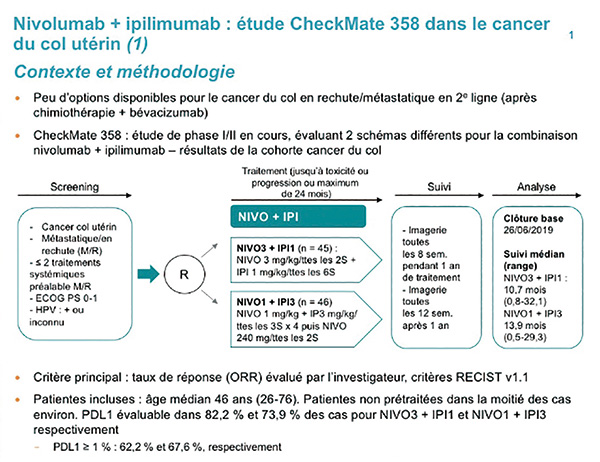
CheckMate 358研究是一项Ⅰ~Ⅱ期开放标签多队列研究,从10个国家30家医院和医学中心入组转移性宫颈癌患者,患者年龄≥18岁,组织学确诊宫颈鳞状细胞癌复发或转移,ECOG PS评分0~1,接受过二线治疗,患者接受纳武利尤单抗240 mg每2周治疗,随机分组患者分别接受纳武利尤单抗3 mg/kg 每2周、伊匹单抗1 mg/kg每6周(NIVO3+IPI1组)或纳武利尤单抗1 mg/kg 每3周、伊匹单抗3mg/kg每3周4周期继以纳武利尤单抗240 mg每2周(NIVO1+IPI3组)。
主要研究终点为研究者评估的客观缓解率,所有接受治疗患者均评估抗肿瘤活性和安全性。
2015年10月至2020年3月,共193例患者入组,176例患者接受了治疗。19例患者接受了纳武利尤单抗单药治疗,45例接受了NIVO3+IPI1治疗,112例接受了NIVO1+IPI3治疗(45例随机队列,67例扩展队列)。
纳武利尤单抗单药组、NIVO3+IPI1组、NIVO1+IPI3组中位随访时间分别为19.9个月、12.6个月、16.7个月,客观缓解率分别为26%、31%、40%(NIVO1+IPI3随机队列)、38%(随机与扩展队列合并)。
最常见3~4级治疗相关不良反应为腹泻、肝细胞溶解、低钠血症、γ-谷氨酰转肽酶升高、脂肪酶升高、呕吐、贫血等,严重治疗相关不良反应发生率在纳武利尤单抗单药组、NIVO3+IPI1组、NIVO1+IPI3组分别为16%、27%、42%,NIVO1+IPI3组有1例因免疫相关结肠炎导致的治疗相关死亡病例。 (编译 王娜)














