GEMSTONE-303研究JAMA杂志正式发表
舒格利单抗GEMSTONE-303研究日前在《美国医学会杂志》(JAMA)正式发表。研究显示,对于既往未经治疗、不可切除、局部晚期或转移性胃或胃食管交界处腺癌患者,舒格利单抗(sugemalimab)联合化疗显著改善总生存(OS)和无进展生存(PFS),差异有统计学显著性及临床意义,安全性可控。(JAMA. 2025年2月24日在线版)
舒格利单抗是全球首个获批用于胃/胃食管结合部(G/GEJ)腺癌的PD-L1单抗,GEMSTONE-303研究结果为其联合化疗作为PD-L1综合阳性评分(CPS)≥5患者新一线标准疗法提供了有力证据支持。

该研究旨在评价舒格利单抗联合卡培他滨和奥沙利铂(CAPOX)一线治疗PD-L1联合阳性评分(CPS)≥5、不可切除、局部晚期或转移性胃或胃食管交界处腺癌患者的疗效,是目前胃癌一线领域唯一将CPS≥5作为cut-off值进行验证的大样本前瞻性研究。
研究纳入符合条件的患者,按1∶1比例随机分配至舒格利单抗+CAPOX组(241例)和安慰剂+CAPOX组(238例)。基于 ECOG PS(0 或 1)和 PD-L1 表达水平(CPS 5~9或≥10)进行分层。主要终点为PFS和OS。次要终点包括客观缓解率(ORR)、缓解持续时间(DoR)及12个月和24个月OS率。
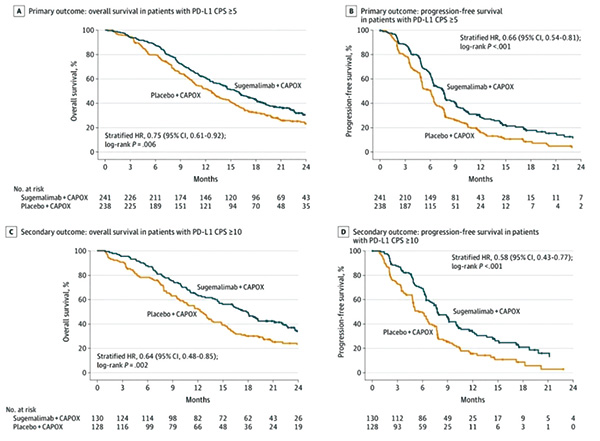
该研究是首项探索PD-L1单抗用于晚期胃癌一线治疗并获得阳性结果的Ⅲ期临床研究,研究达到PFS 和OS双主要终点。舒格利单抗组中位随访时间为25.1个月,安慰剂为26.3个月。舒格利单抗组中位OS(15.6个月 vs. 12.6个月;HR=0.75,95%CI 0.61~0.92,P=0.006)和中位PFS(7.6个月 vs. 6.1个月;HR=0.66,95%CI 0.54~0.81,P<0.001)均显著改善。
在CPS≥10的人群中,PFS 获益更为明显(7.8个月vs. 5.5个月,HR=0.58,P<0.001)。在CPS≥10人群中OS获益更多,中位OS延长5.3个月,死亡风险降低36%(17.8个月vs. 12.5个月,HR=0.64,P=0.002)。舒格利单抗+CAPOX组12个月OS率为61.25%,在CPS≥10的人群中达到63.83%。
舒格利单抗组3级或以上治疗相关不良事件发生率为53.9%,安慰剂组为50.6%。
研究解读
GEMSTONE-303研究主要研究者、北京大学肿瘤医院沈琳教授表示,在PD-1单抗应用于临床之前,化疗用于无法切除的局部晚期或转移性胃/胃食管结合部腺癌患者,其中位OS通常不超过1年。PD-1单抗联合化疗作为新的一线标准疗法已被证明可显著改善晚期胃癌患者的生存,GEMSTONE-303研究在此基础上进一步创新。舒格利单抗作为全球首个在该患者人群中获批的PD-L1单抗,在关键研究设计中果断选择了PD-L1表达人群,显示出了优异的疗效和可控的安全性。研究结果能被JAMA接收并发表是对GEMSTONE-303的创新性以及所有参与人员高质量贡献的印证与肯定。
舒格利单抗是一种非常接近人体的天然G型免疫球蛋白4(IgG4)单抗药物,能降低在患者体内产生免疫原性及相关毒性的潜在风险。目前,中国国家药品监督管理局(NMPA)已批准舒格利单抗五项适应证:联合化疗一线治疗转移性鳞状和非鳞状NSCLC患者;治疗同步或序贯放化疗后未出现疾病进展的、不可切除、Ⅲ期NSCLC患者;治疗复发或难治性结外NK/T细胞淋巴瘤患者;联合氟尿嘧啶类和铂类化疗药物一线治疗不可切除的局部晚期,复发或转移性食管鳞癌患者;联合含氟尿嘧啶类和铂类药物化疗用于表达PD-L1 CPS≥5的不可手术切除的局部晚期或转移性胃及胃食管结合部腺癌的一线治疗。
(编译 赵宏宇)














