2018年AML领域进展盘点
美国MD Anderson癌症中心DiNardo等报告,2018年是AML领域颇具里程碑意义的一年。多种靶向治疗获批,既提供了新的希望也提供了更有效的治疗选择,还强化了基因组分析对患者最佳医疗的重要性。(Nat Rev Clin Oncol. 2019年1月2日在线版 doi: 10.1038/s41571-018-0156-2)
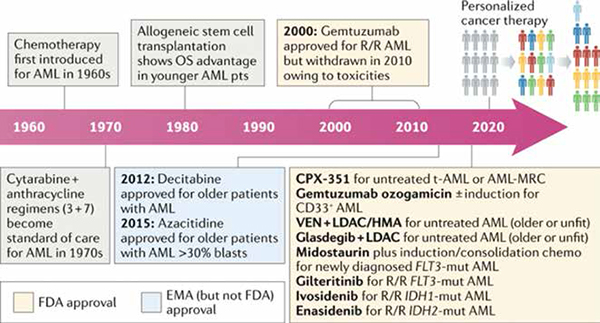
快速且可负担的基因组测序技术,为加深对AML病理生理学的理解带来了契机。2017年是成功收获的一年,获批的项目既有Midostaurin联合7+3化疗治疗FLT3突变AML和Enasidenib治疗IDH2突变AML,又有吉妥珠单抗重新获批和脂质体柔红霉素-阿糖胞苷治疗成人新发的继发性或治疗相关性AML。2018年在AML治疗领域的进展并未让2017年专美于前。
第二代FLT3抑制剂获批
2017年底,多激酶抑制剂Midostaurin联合7+3化疗被批准用于新发的FLT3突变的年轻(<60岁)AML患者是一个开创性的进步。
2018年5月和6月,随着两项第二代FLT3抑制剂结果的公布,Quizartinib获FDA批准用于复发和/或难治性(R/R)FLT3-突变的AML。此外,另一种有效的选择性FLT3抑制剂Gilteritinib也有望获批,目前其在R/R的FLT3-突变型AML患者中Ⅲ期注册试验(NCT02421939)已完成入组。
IDH1抑制剂
AML患者中IDH1突变的发生率约为8%。2014年开始的一项Ⅰ期研究显示,第一个IDH1突变抑制剂Ivosidenib在R/R的IDH1突变型AML(179例)患者中有惊人的疗效,中位OS达9个月。据此,FDA于2018年7月批准了该适应证。
与2017年获批的IDH2抑制剂Enasidenib类似,Ivosidenib有涉及白血病的分化和无细胞毒性的成熟两种独特作用机制,这导致约10%的IDH分化综合征患者需使用皮质类固醇、羟基脲,严重病例甚至可停药。
老年患者中CPX-351的应用
CPX-351是阿糖胞苷和柔红霉素以5︰1固定比例包封的脂质体。一项Ⅲ期研究显示,在符合标准7+3高强度化疗的60~75岁继发性AML或AML伴MDS患者中,CPX-351可改善疗效(48% vs. 33%)和中位总生存期(9.6个月 vs. 6.0个月;HR=0.69,95%CI 0.52~0.90,单侧P=0.003)。
其他治疗进展
针对不宜7+3高强度化疗的老年患者,联用选择性BCL-2抑制剂Venetoclax或Sonic hedgehog(SHH)通路抑制剂Glasdegib可能更有效。FDA最近基于Ⅰ期数据加速了对Venetoclax与去甲基化药物治疗组合的批准,另一项阿扎胞苷联合或不联合Venetoclax对比安慰剂的Ⅲ期确证试验正在进行中。
2018年小剂量阿糖胞苷的应用领域也有诸多重要事件,包括其组合方案在不宜7+3高强度化疗老年AML患者中的应用,联用Glasdegib的获批,联用Venetoclax的加速批准等,均为这一历史难治性患者群提供了另外的治疗选择。
深入了解AML生物学
因为AML具有显著的基因组异质性,所以既往的分析效能不足,无法将复杂的突变模式与治疗反应明确地关联起来。Vizome Beat AML数据查看器是新出现的一个有价值的进展,能在患者水平上自由获取包括治疗结果、全外显子组测序、RNA测序和> 100种药物离体药敏数据在内的详细数据调查,这无疑可加速研究进展,为未来日益个性化和精准化的AML治疗带来希望。
(编译 张威)


