新一代雄激素受体抑制剂安森珂获批
9月10日,强生公司在华制药子公司西安杨森制药有限公司宣布,旗下安森珂(阿帕他胺片)获得国家药品监督管理局加速批准,用于治疗有高危转移风险的非转移性去势抵抗性前列腺癌(NM-CRPC)成年患者。
今年5月,国家药品监督管理局药品审评中心(CDE)因安森珂明显的临床优势授予其“优先审评”资格,并将安森珂纳入第二批临床急需境外新药名单。非转移性去势抵抗性前列腺癌是指药物去势或手术去势后出现前列腺特异性抗原(PSA)进展且通过传统影像学检查未发现远处转移病灶的前列腺癌。临床研究显示,使用安森珂治疗使远处转移或死亡风险降低72%,中位无转移生存期(MFS)可延长两年以上(24.31个月)。
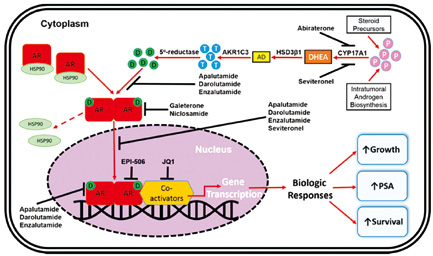
安森珂是中国首个获批用于非转移性去势抵抗性前列腺癌患者的新一代雄激素受体抑制剂。它可阻断前列腺癌细胞中的雄激素信号通路,通过三种途径抑制癌细胞的生长:抑制雄激素与雄激素受体(AR)的结合,抑制活化AR的核转运,以及抑制AR与癌细胞的脱氧核糖核酸(DNA)结合从而阻断AR介导的转录。
安森珂的获批基于一项全球多中心、双盲、随机、安慰剂对照SPARTAN临床试验的Ⅲ期数据。该研究评估了1207例非转移性去势抵抗性前列腺癌患者随机接受每日一次口服安森珂(240 mg)治疗或接受安慰剂治疗的疗效和安全性。
安森珂治疗的患者中位无转移生存期(MFS)有显著改善,达到40.51个月,较之接受安慰剂治疗患者的16.20个月延长了两年以上(24.31个月),发生远处转移或死亡风险降低72% (HR=0.28,95%CI 0.23~0.35,P<0.0001)。其他疗效终点包括至转移时间(TTM)、无进展生存期(PFS)、至症状进展时间均有显著改善。
目前,安森珂已被多个国际前列腺癌治疗指南,作为Ⅰ类或A级推荐用于治疗非转移性去势抵抗性前列腺癌患者。
安森珂于2018年2月14日获得美国食品和药品管理局(FDA)批准用于治疗非转移性去势抵抗性前列腺癌(NM-CRPC)患者,随后在加拿大、澳大利亚、阿根廷、巴西、欧洲和日本等地获得批准。
(编撰 张莉)














