EGFR外显子20插入突变NSCLC EGFR抑制剂CLN-081彰显疗效
会上报告的研究显示,对于多线经治NSCLC患者,CLN-081显示明确的抗肿瘤活性,包括那些既往接受过其他EGFR-TKI治疗后耐药的患者以及基线CNS转移患者。100 mg bid剂量ORR为41%,中位DoR>21个月,中位PFS为12个月。(摘要号 9007)
该研究为表皮生长因子受体(EGFR)20号外显子插入(ex20ins)选择性酪氨酸激酶抑制剂(TKI)CLN-081,用于EGFR ex20ins突变晚期非小细胞肺癌(NSCLC)二线及以上治疗的国际多中心Ⅰ/Ⅱa期研究(NCT04036682),此次又亮相全球肿瘤学大会,公布了最新数据。
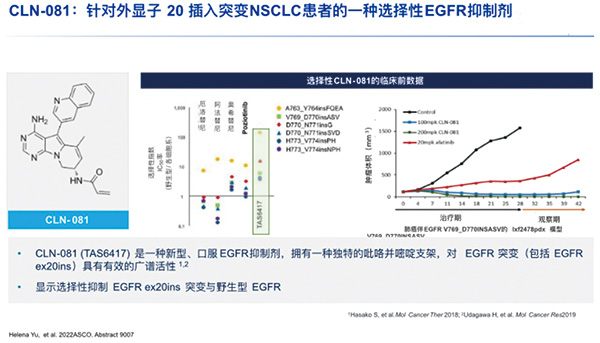
CLN-081是一种新型的口服EGFR-TKI,具有独特的吡咯并嘧啶结构,其特异性支架可安装在EGFR铰链区ATP结合位点上。与EGFR野生型相比,CLN-081对EGFR ex20ins具有选择特异性亲和力,其半数抑制浓度(IC50)比(野生型/突变型)>5倍以上。CLN-081于2022年1月获得美国食品药品监督管理局(FDA)授予“突破性疗法”称号,治疗既往接受过含铂化疗的EGFR ex20ins突变局部晚期或转移性NSCLC患者。
该研究纳入既往接受过含铂化疗的EGFR ex20ins突变复发或转移性NSCLC患者,前期剂量递增和剂量扩展试验确定CLN-081Ⅱ期试验推荐剂量(RP2D)为100 mg bid。入组患者接受CLN-081治疗直至疾病进展、出现不可耐受的毒性或退出试验。治疗6周时、之后每9周评估肿瘤反应(按照RECIST 1.1标准)。
本次数据截至2022年5月9日。共入组73例符合条件的患者,来自美国、新加坡、荷兰、中国共14家中心。目前有24例患者(33%)仍在继续接受CLN-081治疗。
入组患者中位经治线数为2线(1~9线),其中多达66%的患者既往接受过≥2线系统治疗;36%的患者接受过EGFR-TKI治疗;55%的患者接受过免疫治疗;34%的患者基线伴稳定性中枢神经系统(CNS)转移。
39例患者接受RP2D方案治疗,仅2例发生≥3级治疗相关不良事件(TRAEs),包括1例贫血(3%)、1例谷草转氨酶(AST)升高(3%)。最常见的TRAEs为皮疹(83%)、腹泻(36%)、甲沟炎(31%)、疲乏(21%),均为1~2级。治疗减量率和停药率分别为13%和5%。
药代动力学(PK)特征与临床观察结果一致,100 mg BID剂量给药8小时后,药物暴露稳定在EGFR ex20ins突变的GI50(半数抑制浓度)值之上,且暴露在EGFR野生型GI50以上的时间很短。
39例接受100 mg bid治疗患者客观缓解率(ORR)为41.0%(16/39),均为部分缓解(PR);疾病控制率(DCR)高达97.4%(38/39例),仅1例患者出现疾病进展(PD)。中位缓解持续时间(DoR)超过21个月。中位无进展生存(PFS)为12个月。在73例所有患者不同剂量(≤65 mg,100 mg,150 mg)中,中位随访时间为11个月,28例(38.4%)患者达到确认的PR,42例(57.5%)患者达SD,3例(4.1%)PD,mDOR超10个月,中位治疗时间达11个月,中位至缓解时间为1.5个月,mPFS为10个月。
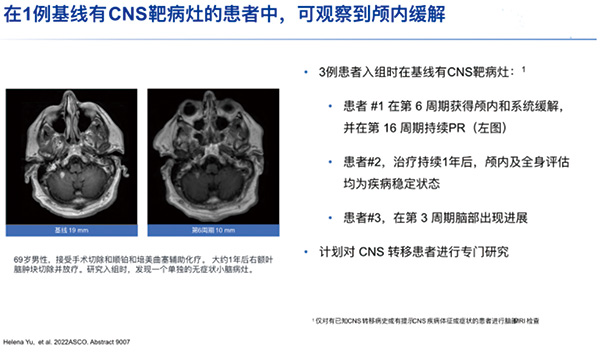
3例患者入组时在基线有CNS靶病灶:分别在第 6 周期获得颅内和系统缓解,并在第 16 周期持续PR;在颅内和全身评估持续SD一年后仍在接受治疗;在第 3 周期脑部出现进展。
CLN-081使用<150 mg bid剂量长期治疗的安全性可接受,绝大多数TRAEs为1~2级,未观察到≥3级的皮疹、腹泻。
随着全球靶向药物研发的进步,EGFR ex20ins靶向治疗近年也迎来重大突破,多类新药相继问世,并取得临床研究进展,包括同时靶向EGFR和c-Met的大分子单克隆抗体Amivantamab、多靶点TKI Poziotinib、同时针对EGFR和HER-2 ex20ins突变的Mobocertinib、DZD9008和仅针对EGFR ex20ins突变的CLN-081、JMT101。其中Amivantamab和Mobocertinib分别于2021年5月和9月先后获得FDA批准用于治疗含铂化疗失败的EGFR ex20ins突变局部晚期或转移性NSCLC患者;CLN-081和DZD9008于2022年初获FDA授予该项适应证的“突破性疗法”称号。这些具有里程碑意义的事件标志着EGFR ex20ins靶向治疗已迈入新纪元。
(编译 胡俊永)














