可切除高危黑色素瘤 mRNA-4157联合帕博利珠单抗显著延长DMFS
澳大利亚伊迪丝考恩大学Khattak报告,与帕博利珠单抗相比,mRNA-4157联合帕博利珠单抗作为可切除的高危黑色素瘤的辅助治疗,可显著延长无远处转移生存期(DMFS)。这些结果进一步证明,个体化新抗原方法对癌症患者有潜在的益处。一项针对黑色素瘤患者的Ⅲ期随机研究将启动。(摘要号 LBA9503)
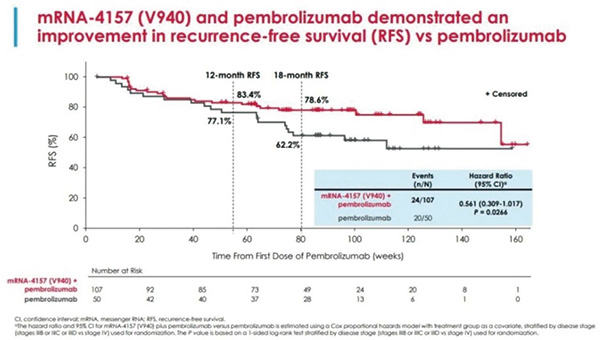
mRNA-4157是一种新型的基于mRNA的个性化癌症疫苗,可编码多达34种患者特异性肿瘤新抗原。该项开放标签随机化Ⅱ期研究(mRNA-4157-P201/Keynote-942)达到了主要终点,即可切除的高危ⅢB/C/D期和Ⅳ期黑色素瘤患者的无复发生存期(RFS)。该研究显示,与帕博利珠单抗单药治疗相比,联合治疗的RFS有统计学意义和临床意义的改善,复发或死亡风险降低44%(HR=0.561,95%CI 0.309~1.017,单侧P=0.0266)。该报告首次分析了DMFS的次要疗效终点。
mRNA-4157-p201是一项正在进行的多中心、开放标签、随机Ⅱ期试验,在完全切除的高危ⅢB/C/D期和Ⅳ期皮肤黑色素瘤患者中进行。患者按2︰1的比例随机分组(按分期分层)接受mRNA-4157联合帕博利珠单抗或单独帕博利珠单抗治疗。
mRNA-4157(1 mg)每3周肌肉注射一次,共9次剂量;帕博利珠单抗(200 mg)每3周静脉给药一次,最长可达18个周期。主要终点是研究者评估的RFS,定义为局部、局部区域、远处复发或新的原发性黑色素瘤。次要终点是预先指定、并在RFS阳性后进行分层评估的DMFS。单侧检验,α=0.99。
157例患者被随机分为mRNA-4157联合帕博利珠单抗组(107例)或帕博利珠单抗单药组(50例)。主要终点的初步分析人群包括所有至少完成12个月研究性治疗的患者,并在观察到44例RFS事件后进行。
在初步分析时,联合组和帕博利珠单抗组的中位随访时间分别为23个月和24个月,联合治疗组中有22.4%(24/107)的患者报告了RFS事件,帕博利珠单抗单药组中有40%(20/50)的患者报告了RFS事件。联合治疗组和单药组的18个月RFS率分别为78.6%(95%CI 69.0%~85.6%)和62.2%(95%CI 46.9%~74.3%)。
与帕博利珠单抗单药治疗相比,联合用药组的DMFS也有统计学和临床意义的显著改善(HR=0.347,95%CI 0.145~0.828,单侧P=0.0063)。8.4%(9/107)和24%(12/50)的患者报告远处复发或死亡,联合治疗组和单药治疗组的18个月DMFS率分别为91.8%(95%CI 84.2%~95.8%)和76.8%(95%CI 61.0%~86.8%)。
这是首次在临床试验中证实mRNA癌症治疗的疗效,研究证据显示,可用癌症疫苗提高手术后高风险黑色素瘤患者无复发生存率。2023年2月,FDA已授予mRNA-4157/V940联合Pembrolizumab的突破性治疗资格,用于辅助治疗完全切除后的高危黑色素瘤患者。基于目前积极的数据,这款疫苗将在2023 年启动针对黑色素瘤的 3 期研究,并计划扩展到肺癌、结直肠癌、头颈癌、子宫内膜癌等其他癌症类型。
(编译 赵梦)














