德曲妥珠单抗治疗中国肺癌患者研究公布
AACR大会上,由吉林省肿瘤医院程颖教授领衔的DESTINY-Lung05试验——重磅抗体偶联药物(ADC)德曲妥珠单抗(trastuzumab deruxtecan)治疗中国肺癌患者数据揭晓,在既往经治HER2突变NSCLC中国患者中实现客观缓解率近60%,疾病控制率超过90%。继德曲妥珠单抗在全球肺癌患者中取得突破后,这款重磅药物 “续写佳绩”,为中国HER2突变肺癌患者带来希望。
德曲妥珠单抗是由人源化抗HER2单克隆抗体通过稳定的可裂解四肽连接子与拓扑异构酶-Ⅰ抑制剂(喜树碱类衍生物DXd)连接组成。德曲妥珠单抗近日获得美国FDA批准具有“不限癌种”适应证,用于既往经治、无法切除或转移性HER2阳性(免疫组化IHC为3+)实体瘤成年患者;此前还获得美国FDA批准用于HER2突变NSCLC、HER2阳性或低表达乳腺癌患者、HER2阳性胃癌和胃食管结合部(GEJ)腺癌患者。
在中国,德曲妥珠单抗已获得中国国家药品监督管理局(NMPA)批准用于HER2阳性或低表达乳腺癌患者;今年稍早时,其用于HER2突变NSCLC的适应证被中国国家药监局药品审评中心(CDE)拟纳入突破性治疗品种和优先审评。
既往DESTINY-Lung02试验表明德曲妥珠单抗在既往经治的HER2突变NSCLC患者中能带来较高缓解率,安全性可控,但DESTINY-Lung02试验尚未覆盖中国患者。DESTINY-Lung05试验正是为了填补这一空白。
此次在AACR上公布的是DESTINY-Lung05试验的主要分析结果。这是一项开放标签、单臂、Ⅱ期试验,在数据截止时(2023年9月23日),共有72例HER2突变NSCLC患者接受德曲妥珠单抗(5.4 mg/kg,每3周1次,为既往验证的有效剂量)。患者中位年龄57岁,41例(56.9%)为女性,22例(30.6%)有吸烟史,其中30例(41.7%)曾接受一线治疗,42例(58.3%)曾接受二线及以上治疗,既往均无HER2靶向治疗史。
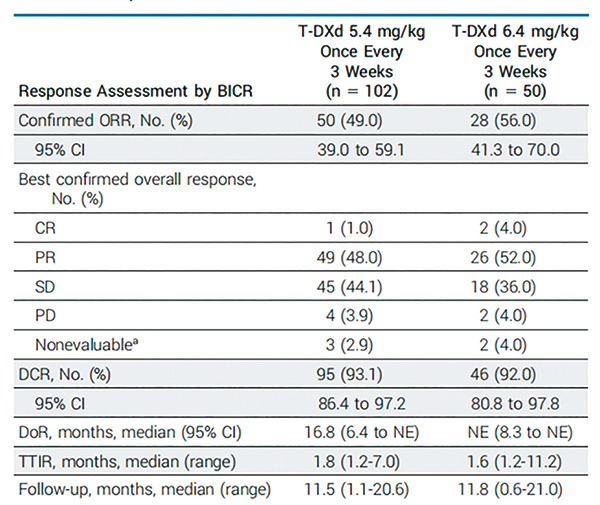
患者的药物暴露中位时间为7.9个月,中位随访时间为9.8个月。多个疗效指标显示德曲妥珠单抗带来了具有临床意义和持久的缓解:客观缓解率(ORR):经ICR(独立中心审查委员会)评估为58.3%(95% CI 46.1%~69.8%),这也是研究的主要终点指标;经INV(研究者)评估数据一致(次要结局之一)。中位缓解持续时间(DOR):经ICR评估尚未达到,经INV评估为9.0个月。

疾病控制率(DCR):经ICR评估为91.7%,经INV评估为93.1%。中位无进展生存期(PFS):经ICR评估尚未达到,经INV评估为10.8个月。1年进展生存生存率:经ICR评估为55.1%,和INV评估为39.7%。
德曲妥珠单抗治疗的安全性可控,且与已知安全性特点一致。共71例患者出现药物相关不良事件(AE),51.4%≥3级。最常见的≥3级AE为:中性粒细胞减少症(26.4%)、血小板减少症(18.1%)和白细胞减少症(11.1%)。2例(2.8%)患者出现导致停药的药物相关AE。17例(23.6%)患者出现严重AE,未出现INV判定的5级AE。经ICR校正后,7例(9.7%)患者发生药物相关的间质性肺病(ILD)/肺炎(6例2级,1例5级)。
总体而言,DESTINY-Lung05试验数据支持德曲妥珠单抗用于既往经治HER2突变NSCLC中国患者, 对于中国及亚洲地区HER2突变转移性NSCLC患者的治疗具有重要的指导意义。 (编译 张嘉佳)














