疫苗联合帕博利珠单抗治疗晚期肝癌
美国约翰斯·霍普金斯大学Yarchoan等报告的Ⅰ/Ⅱ期临床试验显示,个体化治疗性疫苗GNOS-PV02联合PD-1抑制剂用于晚期肝细胞癌(HCC)二线治疗安全性良好,缓解率达30.6%,接近单药治疗历史数据的两倍,总生存期也优于既往单药治疗数据。(Nat Med. 2024, 30: 1044-1053.)
这款疫苗GNOS-PV02以DNA质粒为载体,能编码多达40种新抗原。新抗原指肿瘤基因突变导致肿瘤表达的异常蛋白,而正常宿主细胞中并不会有这些蛋白。通过对患者肿瘤进行测序,可发现每例患者独特的肿瘤突变产生的新抗原,然后将表达这些新抗原的DNA序列导入到DNA质粒中。疫苗注射到体内后,将激发免疫系统生成肿瘤浸润淋巴细胞(TIL)以识别新抗原并杀死肿瘤细胞。
早期研究显示,患者如对肿瘤新抗原具有免疫应答,通常对检查点抑制剂也具有更强烈的应答。这项试验中,研究者选择的治疗策略是,GNOS-PV02、DNA质粒编码的细胞因子IL-12(作为佐剂,强化机体对新抗原的应答)、PD-1抑制剂帕博利珠单抗联用。
试验在36例既往接受过TKI类药物治疗的晚期HCC中开展,至本次数据统计截止日期(2023年8月18日),患者接种疫苗的中位次数为5次(1~18次),中位治疗持续时间为6.1个月。
主要终点为安全性和免疫原性。最常见的治疗相关不良事件是注射部位反应,发生率为41.6%(15例/36例),未观察到剂量限制性毒性或≥3级治疗相关不良事件。未观察到在PD-1抑制剂基础上加用疫苗会降低安全耐受性。
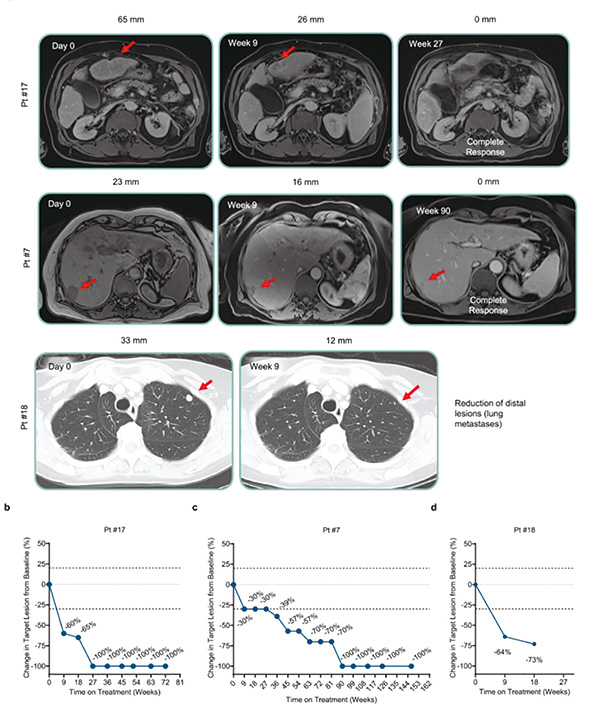
次要终点为治疗效果和可行性。疗效数据支持疫苗联合治疗具有良好的临床活性:分别有3例完全缓解和8例部分缓解,客观缓解率为30.6%(11例/36例),相较于帕博利珠单抗单药治疗缓解率的历史对照值(16.9%,参考自KEYNOTE-240),有统计学显著性。疾病控制率为55.6%(20例/36例)。
起效时间方面,中位至治疗缓解时间为9.3周,中位缓解持续时间未达到。中位无进展生存期为4.2个月,中位总生存期为19.9个月。疾病缓解情况与生存期密切相关。值得一提的是,目前中位总生存期数据优于既往PD-1抑制剂单药二线治疗肝癌的数据(12.9~15.1个月)。
进一步免疫学分析证实了这款疫苗的治疗作用机制。疫苗接种能诱导新抗原特异性应答:22例可评估患者中有19例(86.4%)证实具有新抗原特异性T细胞应答。在14例可评估的患者中,100%在外周血和肿瘤组织中有显著的T细胞克隆扩增。单细胞测序分析显示,这些T细胞克隆绝大多数是CD8 T效应记忆细胞,这是诱导抗肿瘤细胞毒性的关键。2例代表性患者的数据进一步证实了肿瘤浸润T细胞对新抗原具有特异性活性。
总体而言,这项试验结果支持个体化治疗性癌症疫苗能诱导抗肿瘤T细胞生成,且联合帕博利珠单抗治疗具有临床活性。
(编译 张嘉佳)














