新ADC药物温和重建造血系统
瑞士巴塞尔大学Garaudé等开发了一种新的抗体偶联药物(ADC),能有针对性地从白血病患者体内清除所有血细胞同时建立一个新的血液系统,用比造血干细胞移植更温和的方式重建患者的整个造血系统。(Nature. 2024年5月22日在线版)
对于侵袭性白血病患者,治愈的唯一机会就是使用健康的血液系统取代患者的血液系统,即造血干细胞移植。患者需要等待符合配型的移植供体,还要通过化疗清除自身的血液干细胞和大多数血细胞,才能接受供体造血干细胞移植,过程中伴随副作用和并发症风险。高效的抗原特异性细胞耗竭药物模式,例如抗体偶联药物或CAR-T细胞疗法,有望靶向耗竭造血干细胞和肿瘤细胞,从而大大改善造血干细胞移植。不过,肿瘤细胞和其他健康细胞(如造血干细胞和T细胞)共同表达的抗原,导致潜在毒性风险。造血细胞类型的多样性及血液肿瘤细胞表达数百种不同细胞表面抗原的复杂性和异质性,使靶点选择较为困难。
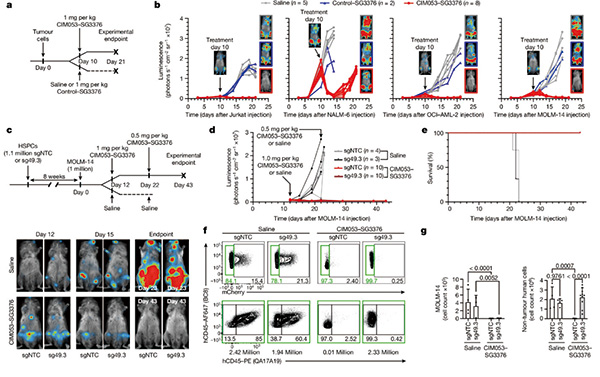
研究者改变了靶点选择的标准,不强调抗原表达的细胞类型特异性,而是找一个广泛表达于所有造血细胞(包括造血干细胞和祖细胞、白血病干细胞和分化细胞)但不在非造血细胞表达的靶点。CD45就是符合这一要求的靶点,CD45仅由造血起源的有核细胞表达,代表了一种泛造血标志物。靶向小鼠CD45的抗体偶联药物可有效耗竭长期重建的造血干细胞,从而实现同种异体造血干细胞移植。
抗体偶联药物是一类具有抗原靶向性的抗体药物,同时具备传统化疗药物的巨大杀伤效应。研究者开发设计了一种高效的抗体偶联药物,以造血细胞上广泛表达的CD45为靶点,可识别患者体内的包括造血干细胞在内的各种血细胞,同时不会识别身体的其他细胞,从而对患病的造血系统进行抗原特异性耗竭。
由于CD45+细胞对造血、免疫防御和许多非免疫功能至关重要,若无额外的预防措施,高效的CD45靶向治疗是难以长期耐受的。在造血干细胞和祖细胞(HSPC)中敲除CD45会导致重度联合免疫缺陷。
研究者此前研究证实,在小鼠CD45中替换一个氨基酸可消除其与单克隆抗体的结合,但不影响其表达和功能。此后,还有研究对人类HSPC进行了工程改造,使其免受抗原特异性治疗的影响,但保留其功能,并维持了植入和多向分化潜能。
为了防止新的造血干细胞及其产生的血细胞受到抗体偶联药物攻击,研究者致力于工程化改造CD45,在其分子中引入一个微小的变化,可在保留其功能的同时,屏蔽靶向CD45的抗体偶联药物,使其对靶向CD45的抗体偶联药物耐药,但保持造血干细胞的功能,从而使靶向治疗成为可能。
小鼠实验证实,靶向泛造血标志物CD45的抗体偶联药物,可特异性地清除整个造血系统,包括造血干细胞(HSC)。将这种抗体偶联药物与经过碱基编辑的人造血干细胞移植相结合,可在选择性清除体内白血病细胞的同时保留移植的造血干细胞的造血功能。
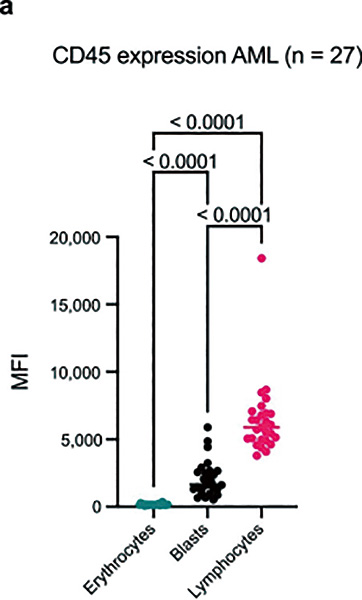
研究者报告了这种新方法在急性髓系白血病动物和体外人类细胞上获得的积极结果。在根除体内恶性肿瘤的同时,动物未出现明显的毒性症状。研究者计划在进一步测试和优化后开始初步的临床试验。研究者认为,这种新方法可为健康状态不适宜为干细胞移植做化疗的患者提供新的治疗选择。
(编译 张嘉佳)














