Amivantamab+拉泽替尼两项初步研究结果

会上公布了Amivantamab和第三代EGFR酪氨酸激酶抑制剂(TKI)联合治疗晚期EGFR突变非小细胞肺癌(NSCLC)的CHRYSALIS研究结果,两项Ⅰ期试验证实了Amivantamab+拉泽替尼靶向治疗的潜力。
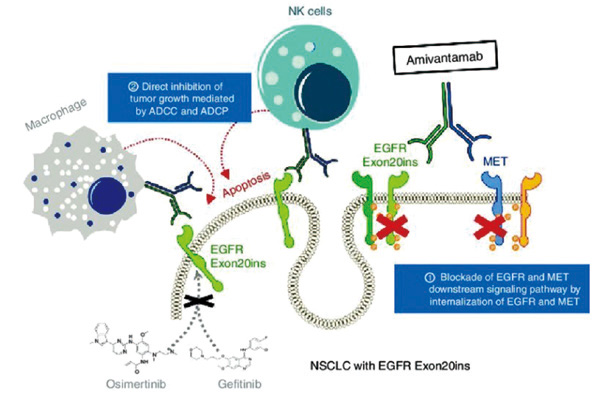
Amivantamab是一款新型的EGFR-MET(间质表皮转化因子)双特异性抗体。正在进行的开放标签Ⅰ期CHRYSALIS研究评估了Amivantamab单药治疗、Amivantamab+拉泽替尼治疗166例奥希替尼治疗进展的EGFR突变NSCLC患者的疗效。(摘要号 1192MO)。
中位随访6.9个月,Amivantamab单药治疗组的客观缓解率(ORR)为19%,临床获益率(CBR)为48%。中位随访11.1个月,联合组报告更高的ORR和CBR,分别为36%和64%。单药治疗组的中位缓解持续时间为5.9个月,联合治疗组为9.6个月。单药治疗组的患者是根据耐药突变(包括C797S)或MET扩增情况进行选择,而联合治疗组的患者是未选择人群和未接受过化疗人群。
第二项正在进行的Ⅰ期试验CHRYSALIS-2研究在136例携带EGFR外显子19缺失或L858R点突变且奥希替尼和铂类化疗(3/4/5线)后疾病进展的患者中评估了Amivantamab+拉泽替尼的疗效(摘要号 1193MO)。
初步结果显示,中位随访时间为4.6个月,29例疗效可评估患者的ORR为41%,CBR为69%;47例经过重度治疗患者ORR为21%。
两项CHRYSALIS试验中,Amivantamab作为单药治疗或与拉泽替尼联合的安全性符合预期,未发现新的安全性信号。
研究解读
两项研究的早期疗效结果以及可接受的安全性数据令人鼓舞。在CHRYSALIS研究中,患者人群未选择的Amivantamab+拉泽替尼组获得较高的ORR和CBR可能出乎意料,但这些数据仍很重要,了解其作用机制非常重要。仍需要对Amivantamab+拉泽替尼联合方案持谨慎态度。在CHRYSALIS-2研究中,重度经治患者的ORR率相对较低,提示该联合方案可能不会改变这一特定患者亚群的临床实践。
两项CHRYSALIS研究仍在进行中,计划分别招募780例和520例受试者。虽然单臂研究的数据非常有用,但随机研究数据是首选,根据耐药突变、治疗线数和是否脑转移进行分层。需要根据耐药机制划分出不同生物标志物驱动肿瘤的患者队列——以了解哪些患者人群将从联合治疗中获得附加价值。 (编译 冯如)














