HR阳性HER2低表达早期乳腺癌 T-DXd新辅助治疗TALENT研究公布

会上报告了TALENT(TRIO-US B-12)Ⅱ期研究旨在评估T-DXd(DS-8201)单药或T-DXd联合内分泌疗法新辅助治疗HR+/HER2低表达早期乳腺癌患者的临床疗效和安全性。(摘要号 GS2-03)
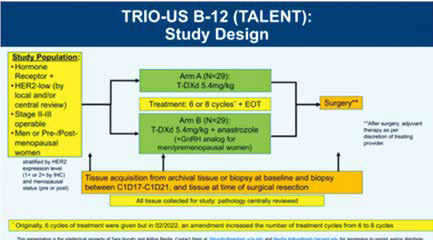
研究纳入既往未接受过治疗,癌灶为可手术的早期浸润性、非复发性病灶,分子亚型为HR+/HER2低表达(IHC 1+或IHC 2+/ISH-),病灶>2 cm的患者。在试验的第1阶段,患者以1∶1的比例随机分配接受T-DXd单药治疗(A组),或T-DXd1联合芳香化酶抑制剂(AI)阿那曲唑治疗(B组)。
根据最初治疗方案,患者共接受6个周期治疗。2022年2月试验治疗方案进行了修订,新入组患者及尚未接受手术的患者,治疗从6周期增加至8周期。此外,随机分配至B组的患者(包括男性患者和绝经前/围绝经期女性患者)也同样接受促性腺激素释放激素(GnRH)激动剂治疗。在T-DXd治疗前、治疗期间和术前采集基线组织活检样本。
研究主要终点为患者手术时的pCR率(ypT0/is ypN0),其他研究终点包括:安全性、客观缓解率(ORR)、Ki67表达变化、残余肿瘤负荷(RCB)指数、探索性生物标志物分析、健康相关生活质量(HRQoL)。
最终,58例患者被随机分配到治疗组。两组之间的基线特征相当;总体而言,大多数患者(约80%)患有HER2低表达疾病,定义为IHC1+,约50%的患者患有淋巴结阳性疾病。
截至2022年10月5日,在疗效方面:A组(29例)完成研究治疗并接受了手术的17例患者中,有1例患者在8个周期治疗后达到pCR(即RCB-0级),2例患者在6个周期治疗后达到RCB-1级(即可见少量病灶残留)。总体而言,达到RCB 0~1级的患者比例为17.6%;B组(29例)完成研究治疗并接受了手术的16例患者中,有1例患者在8个周期治疗后达到RCB-I级。
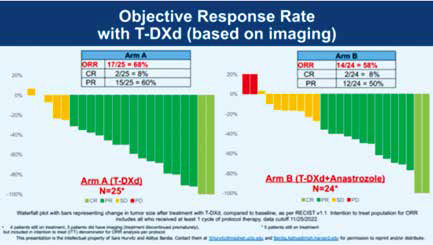
A组可评估患者的ORR为75%(12/16),其中1例为完全缓解(CR)、11例为部分缓解(PR);B组可评估患者的ORR为63.2%(12/19),其中2例为CR、10例为PR,此外B组有1例患者发生疾病进展(PD)。
研究将接受≥1个周期方案治疗的患者纳入意向性分析(ITT),至数据截止日期,A组ORR为68%(17/25),其中2例为CR、15例为PR;B组ORR为58%(14/24),其中2例为CR、12例为PR。
RCB方面,A组24%(7/29)和 B 组31%(9/29) 的患者等待手术结局;A组4例以及B组3例患者提前停药。在HER2表达状态上,T-DXd治疗后49%(17/35) 的患者 HER2 IHC 发生变化,其中大多数患者 (88%) HER2 IHC 表达降低。
安全性方面,有1例患者(1.7%)发生2级间质性肺病(ILD),在停止治疗11天后消退。A组和B组患者最常见的≥3级治疗相关不良事件(AE)包括低钾血症(1.7% vs. 5.2%)、腹泻(3.4% vs. 3.4%)、中性粒细胞减少(3.4% vs. 1.7%)、疲乏(1.7% vs. 3.4%)、头痛(3.4% vs. 1.7%)、呕吐(3.4% vs. 1.7%)、脱水(1.7% vs. 1.7%)和恶心(3.4% vs. 0%)。共有5.2%的患者(3例)因AE需要降低剂量。然而,未报告3~4级肺炎病例,无心肌病或神经病变病例。
T-DXd作为新辅助治疗,在HER2低表达、HR阳性的局限性乳腺癌患者中显示出良好的疗效,并表现出良好的安全性特征,其疗效似乎不受添加内分泌治疗的影响。未来需要进一步证实T-DXd 治疗后观察到 HER2 组织表达的动态变化。
这是T-DXd新辅助治疗HR+、HER2低表达乳腺癌患者的首次报告,为今后抗体药物偶联物用于早期乳腺癌患者的研究提供了基础。据悉,2022年3月,T-DXd在中国的上市申请获 CDE 受理;4月,CDE又接连授予该药突破性疗法认定和优先审评资格;目前其上市申请仍在审评中。 (编译 张萍)














