非小细胞肺癌围手术期全程免疫治疗研究

会上,美国斯坦福大学医学院Wakelee报告了KEYNOTE-671研究的期中分析结果,与接受新辅助化疗和手术的患者相比,接受帕博利珠单抗加顺铂为基础的新辅助治疗,然后接受手术切除和帕博利珠单抗辅助治疗的患者在无事件生存、主要病理学缓解和病理学完全缓解方面有明显改善。(摘要号LBA100;N Engl J Med. 2023年6月3日在线版)
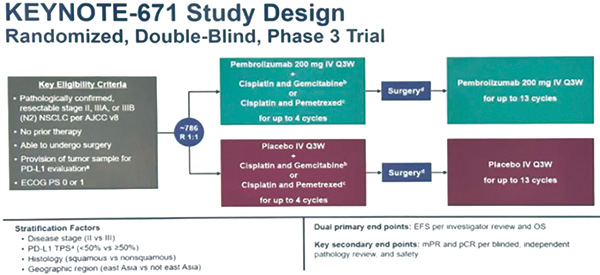
该研究是探讨免疫新辅助联合免疫辅助治疗疗效的随机双盲Ⅲ期临床试验,旨在评估术前帕博利珠单抗+化疗联合术后帕博利珠单抗对早期非小细胞肺癌(NSCLC)患者的疗效。
研究入组797例可切除Ⅱ、ⅢA、ⅢB(N2期)NSCLC患者,1:1比例随机分入帕博利珠单抗组(397例)或安慰剂组(400例)。所有患者治疗分新辅助治疗、手术和辅助治疗三个阶段。
在新辅助治疗阶段,帕博利珠单抗组患者接受帕博利珠单抗(200 mg,每3周1次)联合顺铂+吉西他滨/培美曲塞化疗;安慰剂组患者接受安慰剂(每3周1次)联合顺铂+吉西他滨/培美曲塞化疗。两组在接受最多4个周期的治疗之后,在距离第1周期新辅助治疗不超过20周的时间内接受手术,术后4周后开始辅助治疗。
在辅助治疗阶段,帕博利珠单抗组患者接受不超过13个周期的帕博利珠单抗治疗(200 mg,每3周1次),安慰剂组患者接受不超过13个周期的安慰剂治疗(每3周1次)。主要研究终点分别为无事件生存(EFS)和总生存(OS),次要终点包括主要病理学缓解(MPR)、病理学完全缓解(pCR)和安全性。
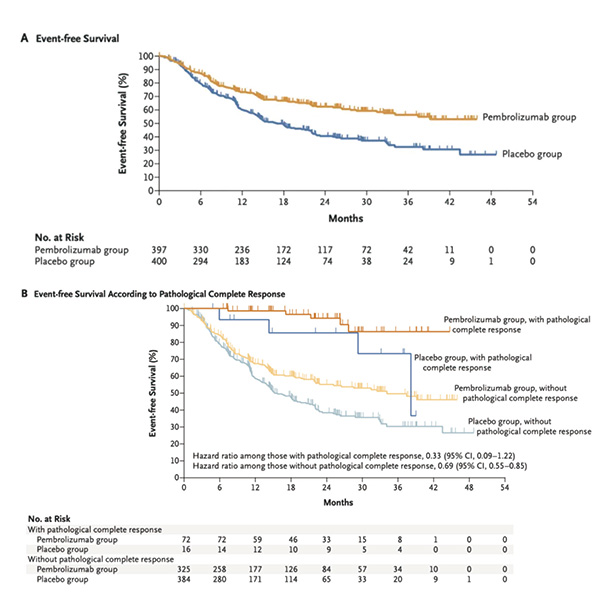
中位25.2个月的随访时间里,共有344例患者(43.2%)发生事件或死亡,大多数事件是疾病进展或复发。安慰剂组患者的24个月无事件生存率为40.6%,中位无事件生存期为17个月,而帕博利珠单抗组患者的24个月无事件生存率为62.4%,中位无事件生存期未达到。与安慰剂组相比,帕博利珠单抗组患者疾病进展、疾病复发或死亡危险降低42%(HR=0.58,P<0.001)。安慰剂组24个月总生存率为77.6%,帕博利珠单抗组为80.9%,总生存数据随访还在继续。
安慰剂组44例(11.0%)达MPR,帕博利珠单抗组120例(30.2%)达MPR;安慰剂组16例(4.0%)达pCR,帕博利珠单抗组72例(18.1%)达pCR。探索性分析显示,无论患者是否达MPR或pCR,帕博利珠单抗治疗均会给无事件生存带来好处。
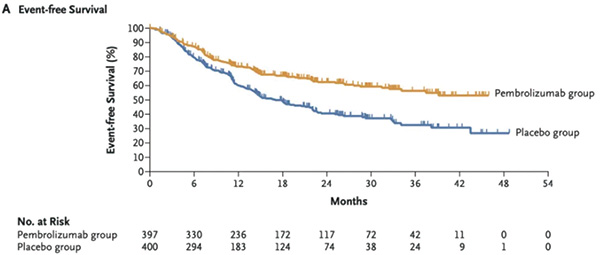
在25.2个月的中位随访时间里,安慰剂组的24个月无事件生存率为40.6%,而帕博利珠单抗组为62.4%。这一数据表明,与安慰剂相比,帕博利珠单抗治疗的早期肺癌患者疾病进展、复发或死亡风险降低42%(HR=0.58,P<0.001)。
帕博利珠单抗组44.9%的患者和安慰剂组37.3%的患者发生3级或以上的治疗相关不良事件。最常见的3级或以上的治疗相关不良事件是中性粒细胞计数减少、贫血、白细胞计数减少和血小板计数减少。
在整个治疗期间,有7例患者因治疗相关的不良事件死亡,其中帕博利珠单抗组有4例(在新辅助-手术阶段,各有1例死于免疫介导的肺部疾病、肺炎和心脏猝死;在辅助治疗阶段1例因心房颤动死亡),安慰剂组3例(在新辅助治疗-手术阶段,急性冠状动脉综合征、肺炎和肺出血各导致1例死亡)。
在讨论部分,研究者比较了KEYNOTE-671与CheckMate 816研究的数据,在仅接受新辅助免疫治疗的CheckMate 816研究中,没有达到pCR的患者疾病进展、疾病复发或死亡的HR值为0.84,而在KEYNOTE-671研究(新辅助免疫+辅助免疫)中这一数据为0.69。不同研究之间的比较虽不够严谨,但也暗示在新辅助免疫治疗后使用辅助免疫治疗或许能进一步提升治疗效果。
(编译 吴曦)














