研究发现肿瘤周围脂肪或能抗癌
美国纪念斯隆·凯特琳癌症中心Sanchez等发现,肥胖肾癌患者肿瘤旁的脂肪里有大量免疫细胞,或是这些患者生存时间较长的原因。[Lancet Oncol. 2020; 21: 283-293. doi: 10.1016/S1470-2045(19)30797-1]

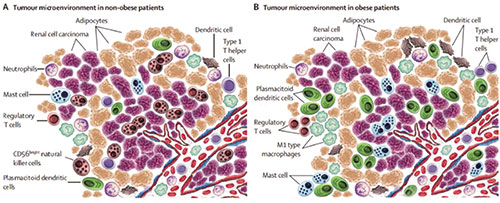
研究发现,肥胖肾癌患者中,肿瘤附近脂肪组织中,免疫细胞浸润和炎症水平明显高于体重正常的患者,肿瘤里也有更多呈递抗原的浆细胞样树突状细胞。可能正是肿瘤周围脂肪聚集的免疫细胞,在各种治疗后被激活,让肥胖的癌症患者有了更好的预后。
肥胖与肿瘤的关系方面,一方面肥胖会增加多种癌症的风险,但患了癌症后,反而往往是肥胖患者治疗效果更好,不管是靶向治疗还是免疫治疗,都是肥胖患者疗效更好,生存时间是体重正常患者的数倍。若能弄清肥胖患者预后更好的原因,或能在肿瘤治疗方面有所助益。
肾癌也是肥胖相关肿瘤,在欧美有30%~40%的肾癌病例是肥胖或超重引起,肥胖肾癌患者较体重正常患者死亡风险降低55%。在肾癌患者中,肥胖患者不仅免疫治疗和靶向治疗效果更好,仅接受手术治疗的早期患者中,也是肥胖者生存时间更长。
为探讨其中缘由,研究者收集了4个队列和一项临床试验数据,包括比较两种靶向药物的COMPARZ试验、研究肿瘤基因组图谱的TCGA队列、研究免疫治疗的MSK免疫治疗队列、前瞻性收集了肾癌肿瘤组织和瘤周脂肪样本的MSK瘤周脂肪队列,以及一个用于评估肿瘤免疫微环境的小队列。研究者对其中体重正常(BMI 18.5~24.9)和肥胖(BMI>30)患者中肥胖与疗效关系的潜在机制进行了研究。
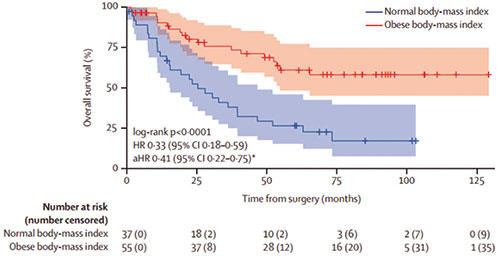
分析发现,无论是使用靶向药物的COMPARZ试验,还是使用免疫治疗的MSK免疫治疗队列,亦或治疗情况未知的TCGA队列,肥胖患者的生存期均显著长于体重正常患者,死亡风险分别低32%、46%和59%。
转录组研究显示,肥胖患者的肿瘤中,缺氧、TGF-β、上皮间充质转化和血管生成相关信号通路明显上调,血管生成评分高于体重正常患者,PD-L1等免疫检查点分子的表达低于体重正常患者。肿瘤突变负荷以及PBRM1、BAP1和TP53基因突变频率均无显著差异。
鉴于肥胖会引起全身性的慢性炎症,研究者着重分析了患者肿瘤和肿瘤周围脂肪组织里各种炎症相关的指标。研究发现,在肿瘤里,肥胖患者的IFN-γ通路表达水平反倒较低,中性粒细胞、巨噬细胞、T细胞等各种免疫细胞的浸润上也均无显著差异,只是浆细胞样树突状细胞较多。
但在肿瘤周围的脂肪里,差异非常显著。肥胖患者肿瘤周围的脂肪组织中,炎性标志物水平明显更高,浸润的免疫细胞也更多。尤其是瘤周脂肪与肿瘤相接的地方,差异更为明显。
研究者猜测,可能正是这些肿瘤周围的脂肪,充当了一个免疫细胞的蓄水池,为抗肿瘤免疫源源不断的提供各种免疫细胞。而在免疫治疗时,脂肪里的免疫细胞也会被激活,发挥更大的抗肿瘤免疫作用。
研究者计划进一步探索BMI在肿瘤预后预测中的价值,并深入研究肿瘤和肿瘤周围脂肪间的相互作用。
(编译 王刚)














