西妥昔单抗成功获批中国头颈鳞癌一线适应证
近期,西妥昔单抗(商品名:爱必妥)成功获批复发转移头颈鳞状细胞癌一线治疗适应证。该适应证在中国的成功获批是基于CHANGE-2研究结果,我国头颈部肿瘤患者多了一种安全有效的治疗选择。
头颈部肿瘤是危害人民健康的重要恶性肿瘤,近年来随着临床研究的进展,复发或转移性头颈部鳞癌治疗领域涌现出多种新的治疗方案和研究证据。从EXTREME到CHANGE-2研究,确立了西妥昔单抗联合化疗一线治疗复发或转移性头颈部鳞癌的地位。
自2008年基于EXTREME研究,西妥昔单抗在全球获批复发或转移性头颈部鳞癌一线适应证以来,目前已使得全球超过45万晚期头颈肿瘤患者接受了含西妥昔单抗方案的治疗,在延长生存的同时改善了患者的生活质量。EXTREME方案(西妥昔单抗+顺铂或卡铂+5FU)已得到多项国内外指南(NCCN, ESMO和CSCO)的一致推荐,用于复发转移头颈鳞癌的一线治疗。
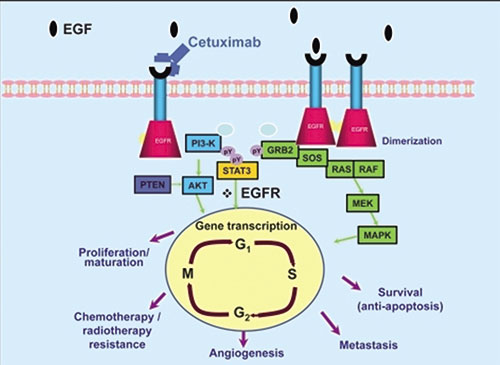
CHANGE-2研究是一项多中心、随机、开放标签、Ⅲ期随机对照试验,主要针对中国复发转移的头颈部鳞癌患者。研究共在全国范围内入组243例组织学确诊为复发/转移头颈部鳞癌的患者,且前期未接受过系统性的全身性化疗。患者随机接受西妥昔单抗+顺铂或卡铂+氟尿嘧啶(西妥昔单抗+PF)治疗,或者使用顺铂或卡铂+氟尿嘧啶(PF)治疗,最多6个周期。在西妥昔单抗治疗组中,疾病没有进展的患者,在化疗后可以接受西妥昔单抗的维持治疗。
经过长期随访,结果显示,在中国复发/转移头颈鳞癌患者中,化疗联合西妥昔单抗可显著改善抗肿瘤活性,患者客观缓解率(ORR)达到50%(对照组为26.6%),同时无进展生存(PFS,5.5个月vs. 4.2个月,HR=0.57)以及总生存(OS,11.1个月vs. 8.9个月,HR=0.69)显著延长。
此外,西妥昔单抗联合化疗组显示出非常好的治疗耐受性和安全性。CHANGE-2研究是一项具有重要里程碑意义的研究。该研究验证了西妥昔单抗在中国复发转移头颈部鳞癌患者中的有效性和安全性,为西妥昔单抗获批治疗中国复发转移头颈部鳞癌患者提供了一个非常强有力的依据。
西方人群和亚洲人群因种族不同,可能在头颈部肿瘤的发病机制以及药物代谢方面存在一定差异。在西方人群中开展的临床研究可能并不一定适用于亚洲人群。在CHANGE-2研究中,研究者通过使用改良的EXTREME化疗方案,证实了西妥昔单抗在亚洲人群中具有良好的疗效和安全性。试验组无论在肿瘤缓解率、无进展生存还是总生存方面都获得了预期结果。
西方发达国家在近20年前就已经使用西妥昔单抗治疗复发转移头颈部鳞癌,但其在国内的适应证仅是针对晚期的结直肠癌患者。同时,由于西妥昔单抗进入医保前价格较高,对经济条件较差的头颈部鳞癌患者来讲有很大的经济压力。
既往调查显示,中国能够负担得起西妥昔单抗价格的晚期头颈部鳞癌患者不足5%。而随着西妥昔单抗头颈鳞癌一线适应证的获批,其有望在今年底进入中国的医保目录,从而使中国复发转移头颈部鳞癌患者接受西妥昔单抗的比例大大增加,提高中国晚期头颈部鳞癌治疗的整体水平。
(编撰 张桦)


