HR+/HER2+早期乳腺癌 降级新辅助治疗安全可行
德国慕尼黑大学附属医院Harbeck等报告的WSG-ADAPT-TP试验表明,激素受体阳性(HR+)/人表皮生长因子受体2阳性(HER2+)的早期乳腺癌(EBC)患者,接受12周无化疗的新辅助降级治疗后,病理完全缓解(pCR)与无需进一步辅助化疗(ACT)者的良好生存相关。(J Clin Oncol. 2023年2月21日在线版)
尽管Trastuzumab-emtansine(T-DM1)联合或不联合内分泌治疗(ET)的pCR率高于曲妥珠单抗联合ET,但由于无pCR后强制标准化疗,所有试验组的结果相似。研究结果证明,在HER2+ EBC中,这种降级疗法对患者是安全可行的。基于生物标志物或分子亚型的患者选择可能会增加全身无化疗HER2靶向疗法的疗效。
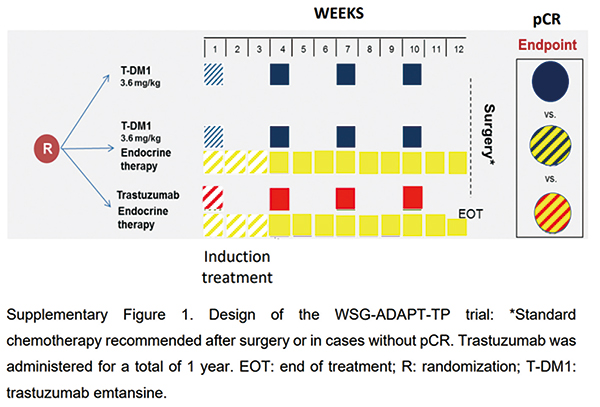
新辅助化疗是HER2+ EBC的标准治疗,与激素受体状态无关。T-DM1是一种抗体药物偶联物,对HER2+ EBC非常有效;然而,在没有常规化疗的情况下,降级抗体药物偶联物为基础的新辅助治疗没有可用的生存数据。
在WSG-ADAPT-TP Ⅱ期试验中,375例HR+/HER2+ EBC(临床Ⅰ~Ⅲ期)患者被按照1︰1︰1的比例随机分配接受12周T-DM1、T-DM1联合ET或曲妥珠单抗联合ET每3周一次。对于pCR的患者,允许省略ACT。该研究报告了次要生存终点和生物标志物分析;对接受至少一剂研究治疗的患者进行分析,采用Kaplan-Meier方法、双侧对数秩统计对生存进行分析,利用Cox回归模型对淋巴结状态和绝经状态进行分层。P<0.05被认为有统计学意义。
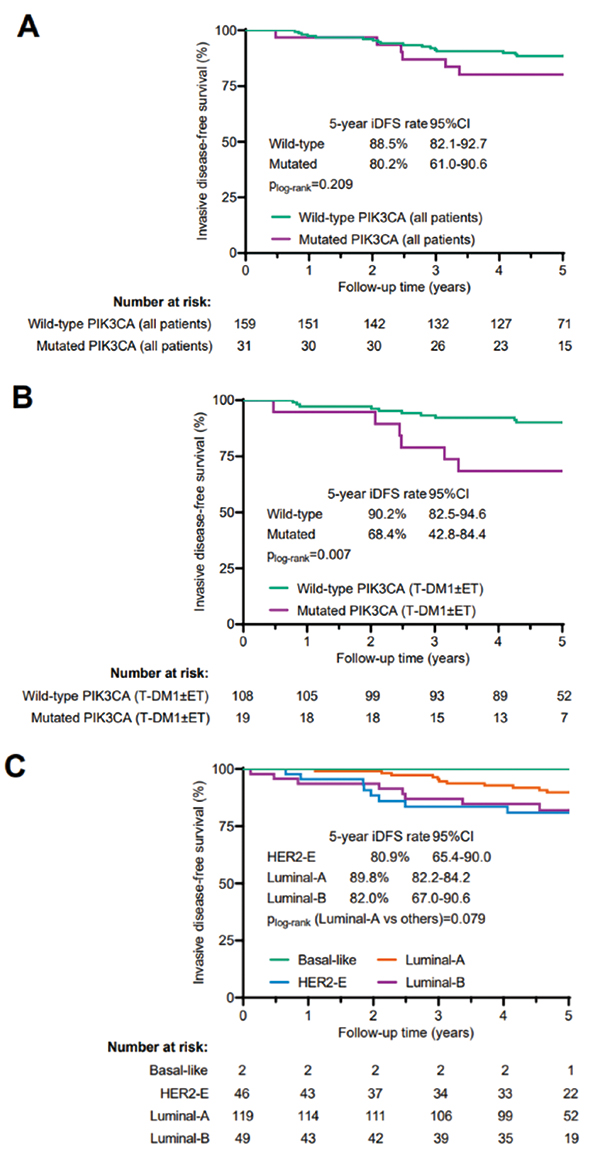
T-DM1、T-DM1联合ET和曲妥珠单抗联合ET诱导了相似的5年无浸润性疾病生存率(iDFS;88.9%,85.3%,84.6%;Plog-rank=0.608)和总生存率(97.2%,96.4%,96.3%;Plog-rank=
0.534)。pCR患者与非pCR患者的5年iDFS率均有改善(92.7% vs. 82.7%;HR=0.40,95%CI 0.18~0.85)。
在117例pCR患者中,41例未接受ACT治疗;接受ACT者和未接受ACT者的5年iDFS率(93.0%,95%CI 84.0%~97.0%;92.1%,95%CI 77.5%~97.4%;Plog-rank=0.848)相似。转化研究显示,PIK3CA野生型、高免疫标志物表达和Lumina A肿瘤(通过PAM50)在降级抗HER2治疗后预后很好。
(编译 崔巧玲)


