局部晚期NSCLC大分割同步化放疗 大剂量自适应SABR瘤床增量或安全有效
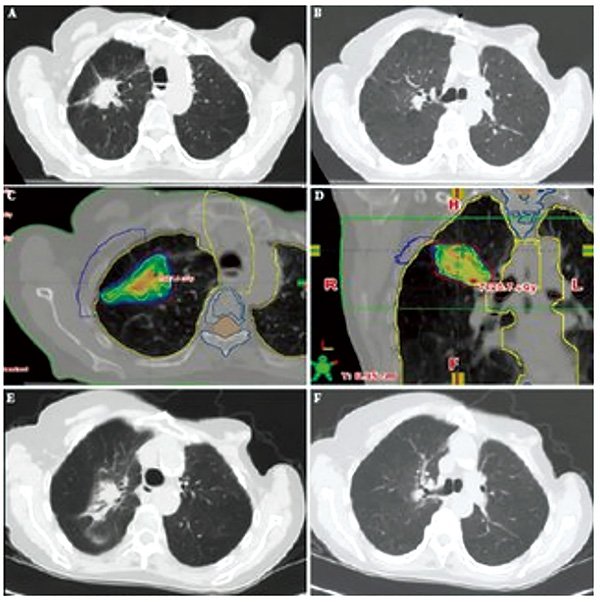
美国加州大学Wu等报告,局部晚期不可切除非小细胞肺癌(NSCLC)患者在大分割同步化放疗时,70 Gy/15 f的自适应立体定向消融放疗(SABR)瘤床增量是安全有效的方案。(JAMA Oncol. 2024年1月11日在线版)
对于局部晚期、不可切除的NSCLC患者,同步化放疗继以免疫检查点抑制剂巩固治疗后,胸腔内进展仍然是主要的失败模式。为了确定大分割同步化放疗和自适应SABR瘤床增量的最大耐受剂量(MTD)和应用情况,该项早期的、单机构、放射剂量递增的、非随机对照试验(HyCRT-SABR)于2011年5月至2018年5月纳入临床Ⅱ期(不可手术/患者拒绝手术)或Ⅲ期的NSCLC患者,给予同步化疗。
中位随访时间为18.2个月。如果在随访的90天内,瘤床增量队列中剂量限制性毒性事件(任何≥3级的肺、胃肠或心脏毒性事件,或任何≥4级非血液学毒性反应事件)发生率<33%,则患者可接受更大剂量的SABR增量。
针对残留的有代谢活性的病灶,所有患者均首先接受10次4 Gy/f的瘤床增量治疗,且还包括额外给予的25 Gy(小剂量,5 Gy × 5 f,总BED10=93.5 Gy)、30 Gy(中剂量,6 Gy × 5 f,总BED10=101 Gy)或35 Gy(大剂量,7 Gy × 5 f,总BED10=108.5 Gy)的瘤床增量放疗并同步卡铂/紫杉醇每周化疗。主要终点为确定MTD。
结果显示,28例患者的数据可评估,其中位年龄为70岁(51~88岁),16例(57%)为男性,24例(86%)患Ⅲ期疾病。小剂量瘤床增量同步化放疗组有患者10例,中剂量瘤床增量同步化放疗组和大剂量瘤床增量同步化放疗组均有9例。方案规定的MTD未达到。
非血液学的近期和晚期(>90天)的≥3级毒性事件发生率分别为11%和7%。中剂量瘤床增量同步化放疗组未见3级毒性事件。大剂量瘤床增量同步化放疗组有2例死亡。小、中、大剂量瘤床增量同步化放疗组的2年局部控制率分别为74.1%、85.7%和100.0%,2年总生存率分别为30.0%、76.2%和55.6%。
研究解读
美国佛蒙特大学拉纳医学院Lester-Coll等评述指出,既往数据提示,生物等效剂量(BED10,包括50 Gy/5 f方案)是否超过100 Gy通常被认为是区分消融性放疗还是治愈性放疗的一个阈值;但Wu等及若干类似方案设计的研究数据则提示,大胆地将BED10的剂量增加到100 Gy,可能为优化局部控制并达到可接受的毒性目的提供了更大的可能性。
当然,这项试验也提出了几个问题。首先,是否有必要采用消融剂量的BED10治疗淋巴结转移灶(通常体积较小)?纵隔淋巴结通常紧邻近端气管、支气管树和食管,这可能会增高严重毒性作用的风险。其次,在更大样本量(目前28例患者)和更长的随访时间(目前中位随访18.2个月)中,尚不清楚化疗后这么快地安排SBRT是否仍然安全。第三,鉴于RTOG 1106的初始报告指出获益不足,尚不清楚与PACIFIC方案相比,该研究是否会改善临床结局。最后,尽管HyCRT-SABR试验中报告的局部控制数据令人印象深刻,但这只是一项没有当代标准放化疗对照的单组试验。
针对不可切除的Ⅱ期或Ⅲ期NSCLC患者,大分割、SBRT和适应性计划的放射剂量递增不太可能是优化结果的唯一方案。在HyCRT-SABR试验中,57%的患者出现了远处进展,这突出表明需要更有效的全身控制来充分实现改善局部控制的益处。将巩固免疫疗法前移到同步甚至新辅助治疗环境中,有可能获得超过在PACIFIC中看到的结局。 (编译 肖丽)














