HER2 CAR-T疗法治疗晚期肉瘤
美国得克萨斯儿童医院Hegde等报告了一种新型HER2特异性CAR-T疗法,治疗晚期肉瘤患者显示安全性和有效性。(Nat Cancer. 2024年4月24日在线版)
肉瘤约占儿童肿瘤的15%,起源于骨骼、肌肉、脂肪等结缔组织。晚期肉瘤治疗选择有限,通常预后较差。目前主要治疗方法有手术、放疗和化疗,不过这些治疗手段往往无法有效控制肿瘤进展。
CAR-T疗法用于实体瘤治疗面临很大挑战,实体瘤复杂的肿瘤微环境,存在多种免疫抑制机制,限制了CAR-T细胞的浸润和杀伤能力。实体瘤抗原表达水平更低,且有异质性,从而使得CAR-T细胞难以识别和靶向肿瘤细胞。
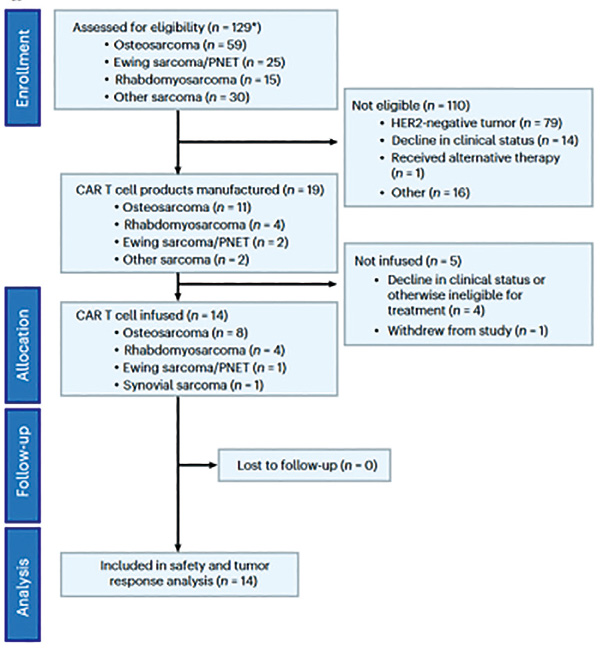
研究团队一直致力于研究HER2 CAR-T疗法。这项开放标签、剂量递增Ⅰ期临床试验设计,旨在评估HER2 CAR-T细胞在淋巴细胞清除后的安全性,次要终点是评估其抗肿瘤活性。该临床试验分为三个治疗组,研究者首先招募患者进入A组,观察安全性。若未出现剂量限制性毒性,则继续招募患者进入B组,使用更强的淋巴细胞清除方案。同样,若未出现剂量限制性毒性,则继续招募患者进入C组,输注更高剂量的CAR-T细胞。临床试验最后选取了14例符合条件的HER2过量表达肉瘤患者。
在氟达拉滨和环磷酰胺联合淋巴细胞清除后,患者可安全耐受高达1×108个HER2 CAR-T细胞/m2的剂量。多数患者出现细胞因子释放综合征(CRS),但均可通过支持性治疗得到控制。未观察到与HER2 CAR-T细胞相关的严重神经毒性或心脏毒性。
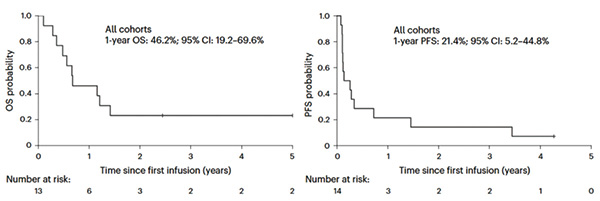
在接受治疗的14例患者中7例(50%)患者疾病稳定或缓解,其中6例(66.6%)患者来自B组。1年生存率为46%,中位随访时间为8.2个月。1例患者在接受多次CAR-T细胞输注后达到完全缓解,并持续缓解超过6年。
与未进行淋巴细胞清除的患者相比,氟达拉滨和环磷酰胺联合淋巴细胞清除可显著提高HER2 CAR-T细胞的扩增和持续时间。淋巴细胞清除在提高CAR-T细胞疗效方面起着关键作用。研究结果显示,淋巴细胞清除可以通过清除体内淋巴细胞,为CAR-T细胞的增殖和扩增创造空间,并调节体内细胞因子水平,从而提高CAR-T细胞的疗效。
尽管CAR-T细胞在体内得到扩增,但多数患者的CAR-T细胞水平在第6周时显著下降。CAR-T细胞在体内的持久性有限,是限制CAR-T细胞疗法治疗实体瘤疗效的主要因素之一。重复输注CAR-T细胞可提高CAR-T细胞的生物利用度,并且耐受性良好。
肿瘤微环境对CAR-T细胞的浸润和杀伤能力也具有重要影响。肿瘤微环境中免疫细胞的丰度和组成与肉瘤类型、CRS严重程度和治疗反应相关。研究者认为,需要进一步研究肿瘤微环境的特征,并开发能克服肿瘤微环境中免疫抑制的CAR-T细胞或联合其他治疗方法。
这项Ⅰ期临床试验表明,在淋巴细胞清除后,自体HER2 CAR-T细胞治疗晚期肉瘤患者是安全的,并具有一定的抗肿瘤活性,这为CAR-T细胞疗法治疗实体瘤带来了新希望。
(编译 张嘉佳)


