呼吸道病毒感染诱导乳腺癌肺转移
美国科罗拉多大学学者研究发现:流感病毒和新型冠状病毒等呼吸道病毒感染诱发的IL-6水平增加,会诱导肺部休眠的乳腺癌播散性癌细胞的表型转变,使其在感染后两周内迅速增殖并成长为转移性病灶;肺CD4+ T细胞通过抑制CD8+ T细胞来帮助维持播散性癌细胞苏醒的有利环境。(Nature. 2025年7月30日在线版)
这一研究发现与英国生物库等大样本队列研究结果一致,新型冠状病毒感染增加肿瘤患者肺转移和死亡风险。呼吸道病毒感染非常常见,仅季节性流感一种,每年感染者超10亿人。病毒性呼吸道感染会引发肺部炎症,伴随IL-6等炎症细胞因子增加和免疫细胞扩增。新型冠状病毒疫情期间,IL-6受体拮抗剂曾是一种治疗方案。肺部病毒感染可通过炎症触发微环境改变,或导致休眠肿瘤细胞的苏醒。
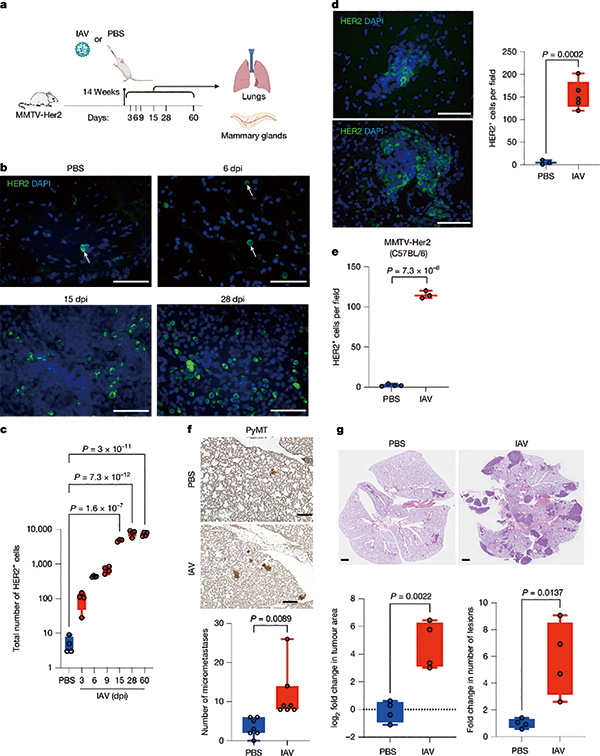
研究者进行了小鼠实验,使用MMTV-Her2乳腺癌转移性休眠小鼠模型,这种小鼠会在10~14周龄时,自然形成散播到肺部和其他器官的播散性癌细胞,可持续存在1年以上,能用于模拟人类肿瘤缓解期的长期休眠状态。
研究者给小鼠感染亚致死剂量的甲型流感病毒,发现在感染后3~15天时,小鼠肺部少量休眠播散性癌细胞簇暴涨100~1000倍,并在长达9个月时间里持续维持高水平。这在其他乳腺癌模型小鼠中也存在,提示流感病毒感染可诱导肺部休眠癌细胞扩增,新冠病毒感染也可唤醒播散性癌细胞。
对播散性癌细胞进行表型分析发现,小鼠感染后,播散性癌细胞从休眠期的间充质样表型逐渐转变为增殖活性增强、免疫逃逸能力提升的表型,提示播散性癌细胞苏醒。唤醒播散性癌细胞的正是流感病毒感染带来的IL-6通路显著激活,IL-6促进了播散性癌细胞的表型转化。敲除模型小鼠的IL-6,病毒感染对播散性癌细胞的影响显著减小,转移灶形成受阻。感染后第15天,小鼠肺部已几乎检测不到IL-6,但播散性癌细胞持续活跃。提示还有其他因素在帮忙维持癌细胞的增殖状态,研究者发现是CD4+ Ti细胞。CD4+ T细胞抑制CD8+ Ti细胞募集和激活,间接保护了苏醒的播散性癌细胞。
研究者分析了英国生物库数据,发现新型冠状病毒感染显著增加了肿瘤幸存者肿瘤相关死亡率(OR=1.82),感染后几个月内死亡风险最高。确诊间隔≥10年的长期缓解肿瘤患者也表现类似趋势,提示依然受病毒感染影响。
Flatiron Health数据库分析结果表明,新型冠状病毒感染后乳腺癌肺转移诊断风险增加(HR=1.44),提示新型冠状病毒感染可能促进了乳腺癌的肺转移。
不过,两年前的另一项研究却有相反的研究发现。浙大研究团队在《自然·免疫学》发表的研究显示,流感病毒感染能训练呼吸道黏膜中的驻留肺泡巨噬细胞,产生持久的抗肿瘤免疫,长久抑制肿瘤细胞的肺转移。这一发现与瘤种有关,或许呼吸道病毒感染和肿瘤转移间的关系比我们想象的要复杂得多。 (编译 赵可心)