盘点目前四大 CDK4/6 抑制剂类药物
近年来,CDK4/6抑制剂正在成为冉冉升起的抗癌“新星”,迅速改变晚期乳腺癌的治疗格局,礼来的阿贝西利片日前在国内正式商业化,继哌柏西利后,国内再迎一款CDK4/6抑制剂。
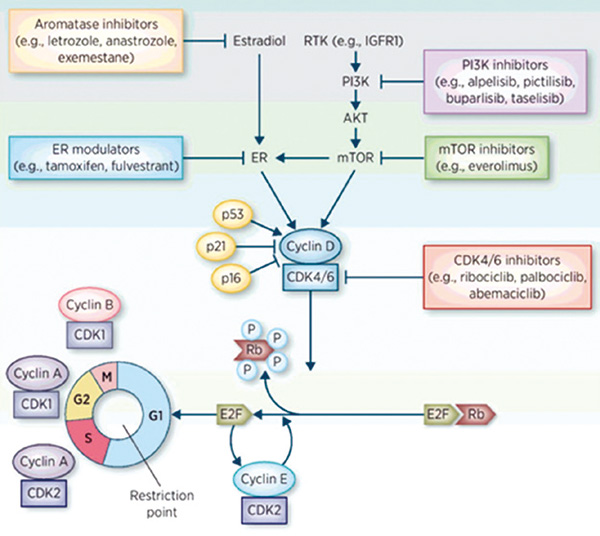
CDK4/6即细胞周期蛋白依赖性激酶4和6,是人体细胞分裂增殖周期的关键条件蛋白,可触发细胞周期从生长期向DNA复制期转变。CDK4/6在很多恶性肿瘤尤其是激素受体(HR)阳性的乳腺癌中过度活跃,表现出显著活性,促使癌细胞增殖扩散,而CDK4/6抑制剂则可将细胞周期阻滞于生长期,从而发挥抑制肿瘤细胞增殖的作用。
目前,全球共批准四款CDK4/6抑制剂,即辉瑞的Palbociclib(Ibrance,哌柏西利)、诺华的Ribociclib(Kisqali,瑞波西利)、礼来的Abemaciclib(Verzenio,阿贝西利)及G1 Therapeutics的Trilaciclib(Cosela),2020年全球市场规模为69.92亿美元。国内目前已获批的CDK4/6抑制剂为哌柏西利和阿贝西利。
哌柏西利
哌柏西利于2015年2月在美国获批上市,作为全球首个获批上市的CDK4/6抑制剂,哌柏西利已成为HR+/HER2-乳腺癌患者一线疗法,目前已获全球90多个国家批准用于HR+/HER2-乳腺癌的一线、二线治疗,占据了大部分CDK4/6抑制剂市场。
根据辉瑞的年度财报,哌柏西利2018年销售额达41.18亿美元,2019年达49.61亿美元,2020年拿下53.92的营收业绩,几乎贡献了辉瑞肿瘤营收一半的业绩。不过基于2023专利到期的危险以及其他竞争对手的出现,其营收增幅从2019年的20%下滑到了9%,地位受到一定的动摇。目前辉瑞正在与印度公司Aurobindo Pharma和Dr Reddy's就哌柏西利进行专利侵权诉讼,并积极拓展哌柏西利新的适应证。
在国内,哌柏西利于2018年7月获得NMPA批准上市,不过目前尚未进入医保。今年1月,辉瑞宣布将对哌柏西利执行新的价格,每瓶售价从29799元降至13667元,降价幅度达到54%。降价同时,辉瑞对此前的患者援助项目做出调整,逐步停止此前针对低保和低收入患者的慈善赠药。
这是哌柏西利在国内上市后的首次降价,业内推测是为了即将迎来的新竞争对手——礼来的阿贝西利做好准备,毕竟此前中国市场中CDK4/6抑制剂只有哌柏西利一款。
生物类似药方面,齐鲁制药的哌柏西利胶囊已在美国获得临时性批准,将于药品专利期到期后正式在美国上市,其在国内已于2020年12月获批上市,成为该品种国内首仿。此外,国内先声药业、奥赛康、豪森、科伦、正大天晴等十余家企业均有布局,其中先声药业已于今年3月报产。
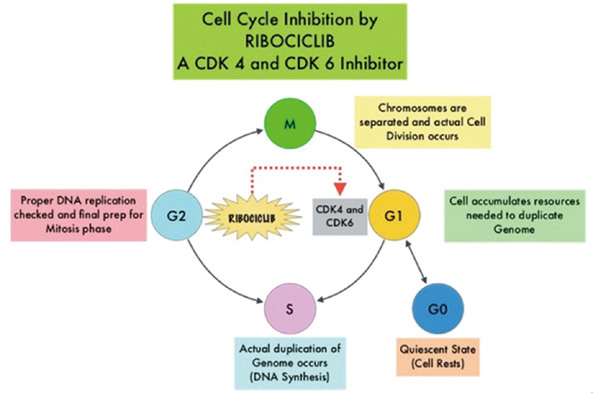
瑞波西利
诺华的瑞波西利于2017年获批,是继哌柏西利之后FDA批准的第二款CDK4/6抑制剂,与芳香酶抑制剂联合作为初始内分泌类治疗方案,用于绝经后激素受体阳性、人类表皮生长因子受体-2阴性(HR+/HER2-)的晚期或转移性乳腺癌女性患者。根据诺华年度财报,瑞波西利2019年销售额达4.8亿美元,2020年达6.87亿美元,增幅为45%。
阿贝西利
阿贝西利(Abemaciclib)是全球第3款上市的CDK4/6抑制剂,于2017年9月在美国获批,主要用于ER+/HER2-晚期或转移性乳腺癌,自上市后其销售额逐年攀升,2019年达到5.8亿美元,2020年达到9.13亿美元,增长57%,成为礼来业绩增长的主要驱动药物之一,并且,基于阿贝西利的增长势头,各家CDK4/6抑制剂的市场份额也将重新划分。
在国内,阿贝西利于2019年11月报产,2020年12月获NMPA批准上市,本月正式面市。
Trilaciclib
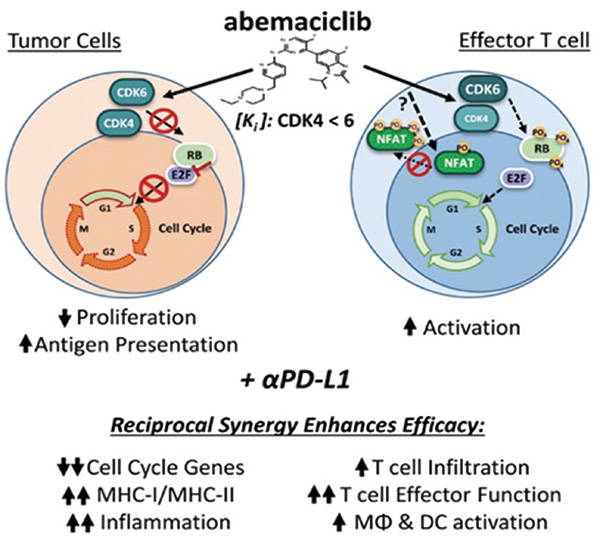
G1 Therapeutics开发的Trilaciclib于今年2月获FDA批准,用于预防扩散期小细胞肺癌成人患者因铂类/依托泊苷方案或拓扑替康方案化学治疗导致的骨髓抑制,同时也是全球唯一一款可降低化疗诱导的骨髓抑制发生率的骨髓保护疗法。
Trilaciclib作为首个短效的小分子CDK4/6抑制剂,G1 Therapeutics将其适应证从乳腺癌转移到了骨髓保护,避开了与已上市的三款CDK4/6抑制剂的竞争。同时,2020年8月,G1 Therapeutics与国内先声药业签署一项金额高达1.7亿美元的独家许可协议,授权先声药业在大中华地区进行Trilaciclib所有适应证的开发和商业化权益。
此外,2020年6月,G1 Therapeutics还与嘉和生物达成了4600万美元的独家许可协议,授权后者在亚太地区(日本除外)进行其另一款CDK4/6抑制剂Lerociclib的开发和商业化,而Lerociclib的主打适应证正是乳腺癌和肺癌。
CDK 4/6作为明星靶点,不少企业都在布局开发,截至2020年2月,全球在研进入临床的CDK4/6抑制剂共有21款,其中有11款属于中国1类新药,恒瑞进度最快,已经开展临床Ⅲ期试验,另有10款研发进度所差无几,均处于临床Ⅰ期研发阶段。 (来源 医谷)


