ASCO:免疫检查点抑制剂治疗相关不良事件管理指南
近日,美国临床肿瘤学会(ASCO)基于最新发表的研究数据对《免疫检查点抑制剂治疗相关毒性的管理指南》进行了更新。(J Clin Oncol. 2021, 39: 4073-4126. DOI: 10.1200/JCO.21.01440)
免疫疗法为不同类型的癌症带来了革命性突破。随着免疫检查点抑制剂(ICPi)在临床中的应用不断深入,适应证不断扩展,作为临床医生,在关注如何精准实施更为有效的免疫治疗策略的同时,也更需注意ICPi安全性的管理。

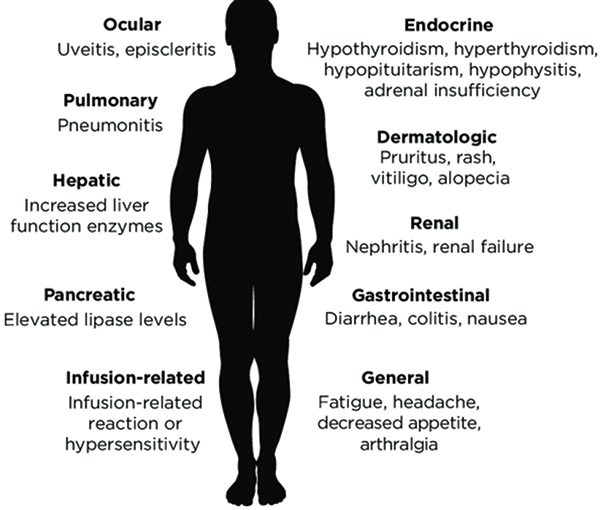
与其他全身疗法如细胞毒性化疗(CTX)截然不同,ICPi引起的免疫相关不良事件(irAE)可能涉及身体的任何器官或系统,胃肠道、皮肤、肝、内分泌和肺毒性较为常见,并且对于发生的任何变化都应该高度怀疑与治疗有关。irAE的发生率因ICPi的类别和剂量、癌症类型以及与患者相关的因素而异。一般来说,接受抗PD-1或PD-L1抗体的患者任何级别irAE的发生率低于接受抗CTLA-4抗体治疗的患者,联合用药会增加irAE的发生率。
出现轻度irAE的情况下继续进行ICPi治疗,并进行密切监测。然而,中度至重度irAE可能损伤器官功能,导致生活质量(QoL)下降,甚至危及生命;因此,了解不同类型生物免疫制剂的irAE,及早发现并妥善管理,对于提高患者生活质量,避免严重irAE的不良结局具有重要意义。
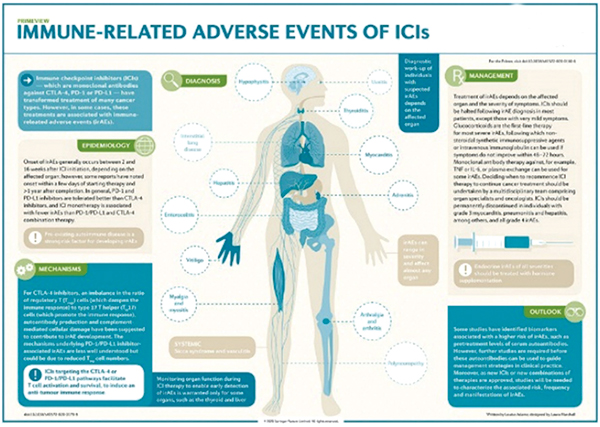
建议临床医生遵循以下建议进行毒性管理:患者和家属护理人员应该在开始治疗前以及整个治疗和生存期内及时接受有关免疫疗法、其作用机制和临床可能发生的irAE等信息的最新教育。对于新出现的症状,应高度怀疑与治疗有关。
一般来说,对于1级毒性(除一些神经、血液学和心脏毒性以外),应在密切监视下继续接受ICPi治疗。
对于大多数2级毒性,可能需要暂停ICPi治疗,并在症状和/或实验室检查的数值恢复至1级或1级以下时考虑恢复治疗,可能施用皮质类固醇(初始剂量为0.5~1 mg/kg/d )。
对于3级毒性,停止ICPi治疗,并开始使用大剂量的皮质类固醇(强的松1~2 mg/kg/d或甲泼尼龙1~2 mg/kg/d)。皮质类固醇的剂量应在至少4~6周的时间内递减。如果在接受大剂量的皮质类固醇治疗48~72小时后症状没有改善,那么对于其中的一些毒性可能需要使用英夫利昔单抗治疗。
当症状和/或实验室检查的数值恢复至1级或1级以下时,可以重新挑战使用ICPi;然而,建议慎重使用,特别是那些早发型irAE的患者。不建议调整治疗剂量。一旦恢复至≤1级,与CTLA-4单抗联合治疗出现毒性的患者可再次使用 PD-1/PD-L1 单药治疗。
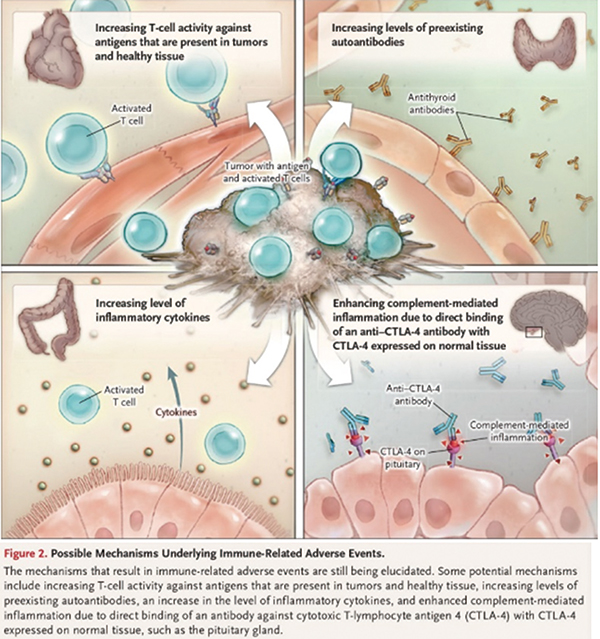
对于4级毒性,一般需要永久中止使用ICPi治疗,除了一些已经通过激素替代得到控制的内分泌毒性以外。
免疫相关皮肤毒性
免疫相关皮肤毒性是ICPi治疗过程最常见的不良事件。根据第4版不良反应事件通用术语标准(CTCAE),免疫相关皮肤AEs包括炎症性皮肤病、大疱性皮肤病和严重皮肤不良反应 (SCAR)。
出现皮肤毒性的中位时间为 4 周,但范围从 2 到 150 周不等。皮疹或炎性皮炎包括多形性红斑、苔藓样、湿疹、银屑病、麻疹样和掌跖红斑感觉障碍或手足综合征。免疫治疗引起的皮疹或炎症性皮炎症状可能不同,但通常包括有或没有皮疹的瘙痒、新的或恶化的皮肤损伤,包括斑点、丘疹或斑块,以及皮肤色素的丧失。对于大疱性皮肤病,出现的症状还可能包括新的或恶化的皮肤病变,包括大疱、持续性荨麻疹或皮肤及黏膜表面的糜烂。
与免疫治疗相关的SCAR包括 Stevens-Johnson 综合征、中毒性表皮坏死松解症、急性全身性发疹性脓疱病(尽管急性全身性发疹性脓疱病并不总是很严重)、嗜酸性粒细胞增多和全身症状或药物过敏综合征的药物反应。免疫治疗引起的SCAR 相关的症状可能还包括发烧、广泛的皮疹、皮肤疼痛、皮肤脱落、面部或上肢水肿、脓疱、水疱或糜烂。
单独使用 CTLA-4 抑制剂或与抗 PD-1单抗联合使用时,皮肤irAE更常发生。虽然皮肤 irAE 可能发生于不同类型的肿瘤患者中,但最常报告于黑色素瘤和非小细胞肺癌 (NSCLC) 。皮肤毒性通常是最早观察到的irAE,在NSCLC与黑色素瘤患者中,注射伊匹单抗后,通常在3周内发生皮肤相关irAE,而在PD-1注射后通常在6周内观察到皮肤相关irAE。即使在治疗完成后,皮肤相关irAE也可能会延迟发生。根据 CTCAE 标准,在 ≤3% 的接受单药治疗的患者中观察到 3 级或更高级别的严重皮肤毒性。尽管皮肤毒性多数较轻,但可能会导致症状负担增加,并影响接受患者的生活质量。
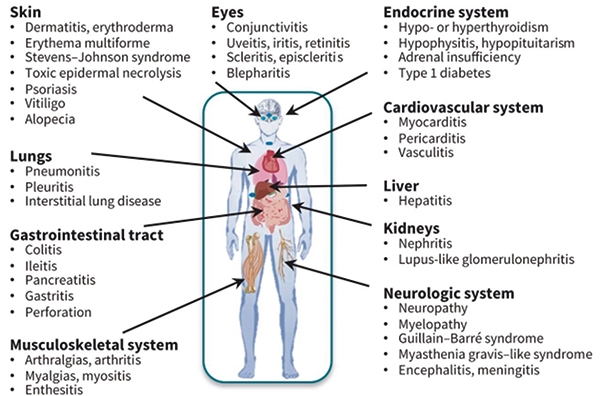
皮肤相关irAE一旦确定,应根据指南邀请皮肤科医生及早参与,给予患者更专业的指导建议,这一点尤为重要。来自大型临床研究的结果表明,皮肤 irAE 可能与临床获益之间存在潜在的相关性,正确识别这些皮肤变化非常重要,以便这些具有良好预后的病例不会停止 ICPi 治疗。
但是,某些表现,包括大疱性皮肤病、和 SCAR如 Stevens-Johnson 综合征以及嗜酸性粒细胞增多和全身症状的药物反应,虽然较为少见,但需要暂时或永久性停止治疗。4级毒性可能需要住院治疗以控制感染风险、缓解症状、伤口处理和补充营养。
虽然许多皮肤 irAE 可以在不永久停止治疗的情况下进行治疗,但irAE 会导致治疗依从性降低、治疗中断或剂量调整。因此,早期识别和对症或系统处理irAE对于提高患者依从性、治疗持续性和最终治疗效果至关重要。
免疫相关胃肠道毒性
免疫相关胃肠道毒性包括结肠炎、肝炎、胃炎和小肠结肠炎。胃肠道毒性发作的中位时间为6 周,范围很广,可以从第1周到107.5 周。ICPi诱发的结肠炎相关症状可能包括腹痛、恶心、腹泻、便血、黏液以及发烧。ICPi 诱发的肝炎相关症状可能包括黄疸、恶心或呕吐、厌食、腹部右侧疼痛、尿色深(茶色)、出血或比正常情况更容易出现瘀伤。
文献中报道的免疫相关结肠炎发生率为8%~27%,在接受抗CTLA-4抗体治疗的患者中腹泻的发生率高达54%,特别是在接受抗CTLA-4 和抗 PD-1 联合治疗时发生率更高。胃肠道毒性在抗 PD-1 单药治疗中较少见,据报道腹泻发生率≤ 19%。大约 1% 的结肠炎患者发生肠穿孔。
尽管与 ICPi 诱发的结肠炎相关的临床因素尚未确定,但据报道,非甾体抗炎药 (NSAID) 的使用与 ICPi 诱发的小肠结肠炎的增加有关,并且在这种情况下使用 NSAID 时应小心。ICPi 诱导的结肠炎和炎症性肠病之间有很多相似之处(例如,临床表现和影像学表现),应注意鉴别。
一旦腹泻达到≥ 2 级,或伴有明显的结肠炎症状,皮质类固醇(1~2 mg/kg)仍然是一线治疗选择。内窥镜可以客观评估结肠炎的严重程度。此外,当免疫疗法与其他全身性肿瘤药物(如 CTX 和酪氨酸激酶抑制剂)联合使用时,鼓励考虑进行内镜检查,这些药物也会引起腹泻。
粪便钙卫蛋白可被视为内窥镜评估的替代或辅助手段。粪便钙卫蛋白的升高已被证明在炎症性肠病中是黏膜损伤的表现,其正常化与黏膜愈合有关。应该注意的是,对于涉及胃肠道的恶性肿瘤,由于存在与癌症相关的管腔炎症,已观察到粪便钙卫蛋白升高。
对于轻度腹泻(1 级),建议单独保守治疗,短期使用任何免疫抑制剂(包括布地奈德等外用形式)均应谨慎,因为缺乏对其有效性的支持证据。对于初始皮质类固醇和随后的英夫利昔单抗或维多珠单抗难治的中度或重度结肠炎患者,已有报告其他替代医疗选择(托法替尼和优特克单抗),但是样本量非常小。粪便微生物群移植也被证明在治疗 15 例难治性结肠炎病例中达到 75% 的疗效。初步数据表明,与其他免疫疗法治疗的患者相比,胃肠道毒性与生存率和治疗结果改善相关。
与下胃肠道毒性相比,上胃肠道毒性比较少见,主要为吞咽困难、恶心或呕吐以及上腹痛。可通过组织活检发现片状慢性十二指肠炎或慢性胃炎伴罕见肉芽肿。治疗策略类似于结肠炎,对于难治性病例,先使用皮质类固醇,然后使用英夫利昔单抗或维多珠单抗。
据报道,在接受伊匹单抗、纳武利尤单抗和帕博利珠单抗单药治疗的患者中,有2%~10%的患者发生了肝毒性。伊匹单抗联合纳武利尤单抗全级别肝炎的发生率为25%~30%, 3 级毒性的发生率约为15%。主要在治疗开始后的6~12 周内发生。如果血液检查或影像学评估没有确定,则应考虑进行肝活检以排除持续性或难治性肝炎的其他病因。
对于皮质类固醇难治性病例,在一项成功的病例研究中报道可以使用吗替麦考酚酯。考虑到肝毒性,不推荐使用肿瘤坏死因子 α 阻滞剂英夫利昔单抗。其他替代免疫抑制剂仍需要进一步的证据以证明其有效性和安全性。
既往肝炎患者出现ICPi 诱发的结肠炎的情况很少见,这也代表了在毒性管理上存在挑战,这类患者可用的选择更为有限,应考虑包括永久停止抗 CTLA-4 和其他可能的 ICPi 治疗。
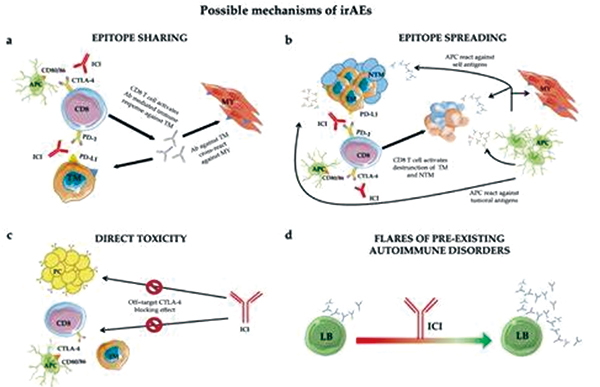
文献中也很少报道有症状的胰腺炎,不建议对无症状患者进行淀粉酶或脂肪酶的常规监测,如果患者在因肿瘤评估等其他原因进行的检查中出现提示性症状或可疑发现,则应开始对胰腺炎及其潜在原因进行检查。皮质类固醇在治疗 ICPi 介导的胰腺炎或胰酶升高中的作用尚未明确定义,但在排除 ICPi 诱发的 irAE 以外的病因后,可以考虑在有症状的疾病中使用皮质类固醇。
后续内窥镜检查显示黏膜愈合,或粪便钙卫蛋白水平≤ 116 μg/g,可被视为指导ICPi 恢复治疗的潜在参数,以最大限度地降低结肠炎复发的风险。肝炎和胰腺炎等毒性也有一定的复发风险。这些最常见于ICPi 应用早期,且通常是低级别的,可以通过标准治疗来控制。尽管如此,应注意确保实施适当的监测和管理策略。
免疫相关肺毒性
免疫相关肺炎是一种不常见但潜在的严重毒性。在抗 PD-1/PD-L1 相关的研究中报告的肺炎发生率从 0% 到 10%,最近对 20 项 PD-1 研究的荟萃分析报告肺炎的总发生率为 2.7%。抗 CTLA-4 治疗导致的肺炎不常见,在接受伊匹单抗治疗的试验中报告肺炎的发生率不到 1%。免疫联合治疗相比单药治疗肺炎的发生率更高(10% vs. 3%)。并且与接受单药治疗的患者相比,接受联合治疗的患者irAE 更难管理。新数据表明,大约 2% 的具有免疫相关毒性的 NSCLC 或黑色素瘤患者出现了慢性肺炎,尽管已经停药,但这种毒性仍然存在,并且在使用皮质类固醇 > 3 个月后可能不会消退。
不同肿瘤类型发生ICPi 相关肺炎和肺炎相关死亡风险仍不明确。根据 Nishino 等人的荟萃分析,NSCLC 发生全级别肺炎的几率高于黑色素瘤患者(OR=1.43)。同样,肾细胞癌 (RCC) 患者也比黑色素瘤患者更容易患全级别肺炎(OR=1.59)。相比之下,其他研究报告的3~4 级肺炎发生率在不同肿瘤类型相似,但在 NSCLC 患者中观察到的肺炎与治疗相关的死亡人数更多。在一项多中心、大型、回顾性分析显示,曾经或现在吸烟者 (56%) 和从不吸烟者 (44%) 都报告了肺炎。最新证据还表明,在接受胸部放疗和检查点抑制剂治疗的患者中,包括肺炎在内的 irAE 发生率无显著差异。
磨玻璃影或斑片状结节浸润,主要分布于下叶是ICPi 相关肺炎胸部影像的常见表现。通常报告为局灶性,与靶向药物相关的弥漫性肺炎不同。Naidoo 等报告了五种不同的影像学亚型:慢性阻塞性肺炎样、磨玻璃样混浊、超敏反应型、间质型和未另作说明的肺炎。
当临床表现与肺炎一致时,经支气管活检的作用目前还存在争议,通常不需要。活检可能有助于排除其他病因,如肿瘤或感染性的淋巴管扩散,或区分慢性 ICPi 肺炎,应在仔细评估风险-获益后决定是否进行活检。
推荐使用皮质类固醇治疗作为初始治疗有症状的 ICPi 肺炎患者,研究显示超过 80%的病例临床症状得到改善。如果皮质类固醇治疗48小时后症状未得到改善则被认为是类固醇难治性,此时没有标准的免疫抑制疗法。根据两项大型回顾性研究,可以选择英夫利昔单抗、霉酚酸酯、静脉注射免疫球蛋白 (IVIG) 或环磷酰胺。
除了肺炎的典型表现外,结节样肉芽肿反应——包括胸膜下微结节混浊和肺门淋巴结肿大,以及胸腔积液——都与 CTLA-4 和 PD-1/PD-L1 治疗有关。临床表现多样,患者可能出现包括咳嗽、气喘、疲劳、胸痛、或无任何症状。由于临床表现不同,临床医生应谨慎诊断此类免疫相关肺炎,活检可能有助于确诊。
免疫相关内分泌毒性
免疫检查点抑制剂治疗相关的内分泌不良事件可给非内分泌科医生带来独特的临床挑战,有症状或实验室检查结果异常的患者有发生中枢性和原发性内分泌功能异常的可能性。一项纳入 38 项随机试验的 7551 例患者的系统评价和荟萃分析显示,接受ICPi治疗的患者出现有临床意义的内分泌疾病的总体发生率约为10%。多种治疗方法和联合治疗的器官靶向率各异,例如,垂体炎在使用伊匹单抗时最常见。随着 ICPi 的使用变得更加广泛,任何内分泌器官都有可能成为 irAE 的目标。
需要对主要激素和相应垂体激素进行临床测量来定位疾病,并且需要早晨血清激素值。例如,早晨皮质醇低表明肾上腺功能不全,但并不代表问题出现在垂体还是肾上腺。如果同时测量的促肾上腺皮质激素 (ACTH) 低,则提示垂体炎、垂体肿块或医源性原因;在原发性肾上腺皮质功能不全中,晨起ACTH 会升高。
这同样适用于评估甲状腺功能,临床医生通常使用垂体激素而不是主要激素进行筛查。低促甲状腺激素 (TSH) 可能与甲亢或中枢性甲减一致;所以,需要游离甲状腺素 (FT4) 水平来确认诊断。当患者有症状并且怀疑有甲状腺功能减退时,同时检测TSH 和 FT4 尤为重要,因为在垂体炎中,TSH 可以保持在实验室检测的参考范围内,但由于垂体疾病导致糖基化改变而失去功能,因此只有FT4 会发现甲状腺功能减退症的存在。
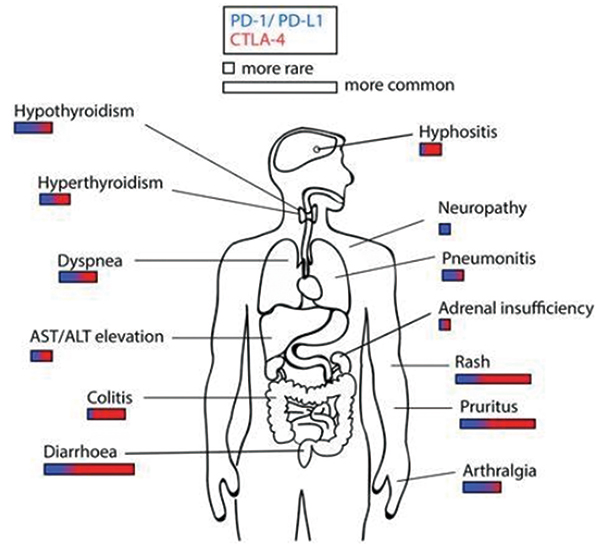
区分原发性和继发性激素问题对于确保患者得到适当的治疗是必要的。例如,当多种垂体激素缺失时,需优先给予氢化可的松来预防激素替代造成的伤害,避免肾上腺危象的发生。同样,在大多数原发性肾上腺皮质功能不全的情况下,除了氢化可的松之外,还需要氟氢可的松,这涉及盐皮质激素的损失以及肾上腺产生的糖皮质激素,导致更严重的血压和电解质异常,但对于继发性或中枢性肾上腺皮质功能不全者常没有必要。垂体激素不是监测中枢疾病状态的可靠指标,特别是 TSH 对监测中枢性甲状腺功能减退症患者的左旋甲状腺素治疗没有帮助,应改用 FT4。
由于伴随急性疾病激素水平的生理变化以及影响垂体功能的药物的使用可能会影响内分泌功能障碍的诊断。与接受 ICPi 的患者最相关的是皮质类固醇的使用。大剂量皮质类固醇会抑制 ACTH 并在停止治疗时可能导致持续性中枢肾上腺功能不全,需要数周到数月的时间才能恢复,具体取决于暴露时间的长短。
当患者接受皮质类固醇治疗时,不应常规测量血清皮质醇水平。如果对疑似肾上腺危象进行急性治疗后,可以进行 ACTH 刺激试验以帮助诊断。内源性水平也可以在最后一剂生理性氢化可的松替代物后 24 小时直接测量,以评估功能恢复情况。大剂量皮质类固醇和对急性非甲状腺疾病的生理反应可导致低 T3 综合征,伴有 TSH 的中枢抑制或轻度升高,但尚未显示出治疗有益。
免疫治疗可引起免疫功能紊乱,使胰岛素持久性缺乏,发生 1 型糖尿病。尽管ICPi相关糖尿病 (CIADM) 发生率较低,但仍需要警惕。既往无2 型糖尿病危险因素的患者新发高血糖应警惕CIADM。急性发作的多尿、烦渴、体重减轻和嗜睡是糖尿病的特征性表现,应立即进行评估。尿酮体、酸碱状态和电解质可作为酮症酸中毒(DKA)筛查和住院评估。还应进行抗体、胰岛素和 C 肽水平检查以支持诊断,但不应因等待结果而推迟治疗。任何诊断有问题的患者都应使用胰岛素治疗高血糖症。目前,尚无免疫抑制策略被批准用于治疗 1 型糖尿病,因此不考虑在 CIADM 中使用。
免疫相关骨关节和肌毒性
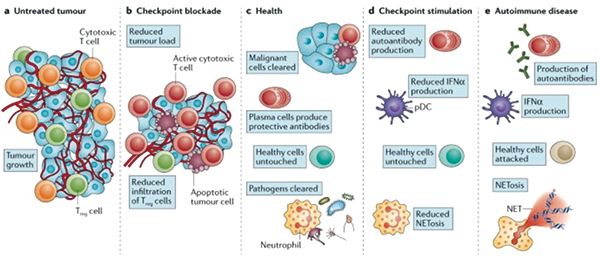
在接受 ICPi 治疗的患者中,关节痛和肌痛等肌肉骨骼症状十分常见,临床研究报道发病率可达40%,严重影响患者的生活质量。最常见的是骨关节/肌肉类风湿样改变,如关节炎、多肌痛样综合征和肌炎等。CTLA-4 或 PD-1/PD-L1 单抗均可出现此类反应,更多见于PD-1/PD-L1 单抗以及联合治疗时。
继发于 ICPi 的免疫相关关节炎患者的临床表现可能会有所不同并影响大关节和/或小关节。关节炎可能在治疗期间的任何时间发生,一些患者在开始 ICPi 治疗数月后首次出现症状。最常见的鉴别诊断包括退行性关节病、骨关节炎和软组织风湿病,如肩袖肌腱炎、晶体关节病(痛风和假痛风)和化脓性关节炎。
先前患有晶体性关节炎、软组织风湿综合征和骨关节炎的患者在 ICPi治疗期间也可能发作。ICPi诱导的关节炎患者的炎症标志物通常非常高,可用于鉴别诊断。单独使用非甾体抗炎药通常不足以控制症状,可能需要皮质类固醇和合成/生物缓解疾病的抗风湿药。如果只有一个或两个关节受到影响,关节内注射皮质类固醇是一种选择。
接受 ICPi 的患者可在其近端上肢和下肢出现严重的肌痛,以及类似于风湿性多肌痛的严重疲劳,也可能出现关节痛。超声或磁共振成像 (MRI) 也可能显示肩关节有轻度积液。患有多肌痛样综合征的患者有疼痛但不是真正的虚弱。鉴别诊断包括炎性肌炎、纤维肌痛、他汀类药物诱发的肌病和其他类型的关节炎或软组织风湿综合征。类风湿因子和抗瓜氨酸蛋白抗体阴性,炎症标志物高度升高。肌酸激酶 (CK) 水平通常应在正常范围内,可以与肌炎鉴别。
肌炎是ICPi的一种罕见并发症,但可能导致严重后果,甚至致命。抗 PD-1/PD-L1 比抗 CTLA-4 药物更常见。可以表现为先前存在的副肿瘤性多肌炎或皮肌炎的再激活,或表现为新发性肌炎。炎性肌炎的主要症状是虚弱,主要表现为四肢近端,站立、举起手臂和四处走动都有困难。严重时患者也会出现肌痛。新发性肌炎患者不会出现副肿瘤性皮肌炎所见的典型皮疹。肌炎可具有横纹肌溶解的暴发性坏死病程,并可累及心肌,在这种情况下,需要紧急治疗以避免致命的并发症。伴有心肌炎和/或重症肌无力的患者预后不良,死亡率高。
免疫相关肾毒性
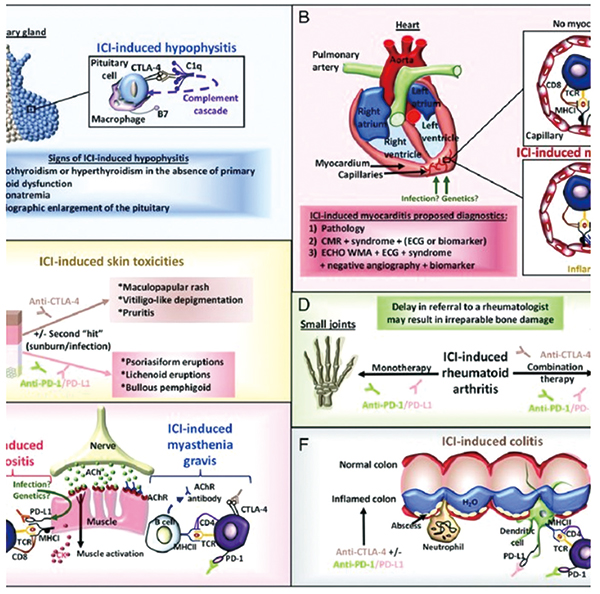
免疫相关肾毒性包括肾炎或急性肾损伤 (AKI)。AKI 是免疫治疗的罕见并发症。初步研究估计,在接受单药 ICPi 治疗的患者中,任何级别 AKI 的发生率为 1%~2%,在接受抗 CTLA-4 和抗 PD-1 联合治疗的患者中为 4.5%。单药组 3 或 4 级 AKI 的发生率 < 1%,联合 ICPi 的发生率为 1.6%。新数据表明,ICPi 的 AKI 发生率更高(范围为 9.9%~29%),通常为1级,主要表现为电解质紊乱而非肾功能下降。
在每次应用ICPi 前,患者应检查血清肌酐。对于肌酐新升高的患者,应考虑暂停治疗,同时评估其他潜在原因(例如,近期静脉注射放射造影剂、脱水、其他肾毒性药物,包括伴随的 CTX 和尿路感染)。无其他明显原因或对替代治疗措施无反应的患者应确定为具有免疫相关的肾毒性并进行经验性治疗。除非 AKI 对类固醇和其他免疫抑制剂无效,否则通常不需要或不建议进行肾活检。
免疫相关神经毒性
免疫相关神经系统毒性最初报告的发生率为 1%;然而,最近的分析显示越来越常见。对 59 项试验共 9208 例患者的分析报告显示,接受抗 CTLA-4 抗体治疗的患者神经系统 irAE 的总发生率为 3.8%,接受抗 PD-1 抗体治疗的患者为 6.1%,接受抗 PD-1 抗体联合抗 CTLA-4 抗体治疗的患者为 12.0%。但3 级和 4 级 irAE 的发生率 < 1%。一项单一机构的回顾性研究发现,在 1834 例接受 ICPi 治疗的患者中,严重(3 级或更高)神经系统 irAE 的真实发生率为 1.5%。周围神经系统比中枢神经系统更易受到影响。神经系统 irAE 以及心肌炎的死亡率高于其他 irAE。
诊断ICPi 相关的神经系统毒性其他病因导致的中枢和周围神经系统症状,如肿瘤进展、癫痫、感染和代谢紊乱以及副肿瘤性神经系统综合征和自身免疫性脑病。对于出现头痛(单独而言,可能提示无菌性脑膜炎)的患者,重要的是评估其意识模糊状况、行为改变、失语、癫痫样活动或短期记忆丧失,其中任何一个表现都可能提示脑炎。
对于大多数神经系统 irAE,诊断性检查应包括 MRI 脑和/或脊柱成像和脑脊液分析,包括细胞学检查以排除软脑膜转移。脑脊液分析有助于临床评估脑炎、无菌性脑膜炎和感觉运动神经病或格林-巴利综合征,在多数情况下显示淋巴细胞增多和蛋白质升高。在无菌性脑膜炎、脑炎和感觉运动神经病中可能会出现神经影像学上的异常软脑膜增强,这凸显了CSF 细胞学检查的重要性,该检查应为阴性。神经传导研究和 EMG 可能有助于诊断感觉障碍或减弱。自主神经病变可能与其他神经病变症状同时发生,应进行筛查。
免疫相关血液毒性
免疫相关血液学毒性并不多见。随着 ICPi 应用的增加和对血液学毒性认识的提高,预计血液学毒性病例会增加,从而需要加强临床管理。对 WHO 药物警戒数据库的调查发现,溶血性贫血以及免疫性血小板减少症 (ITP) 是最常见的血液学毒性,中位发生时间为 40 天。
免疫治疗引起的溶血性贫血患者可能会出现虚弱、苍白、黄疸、深色尿、发热和心脏杂音。免疫相关血栓性血小板减少性紫癜(TTP)可表现为发热、轻度肾功能衰竭和神经系统表现,如癫痫发作、偏瘫和视力障碍。免疫治疗引起的溶血性尿毒症综合征相关的症状可能包括血性腹泻、排尿减少或血尿、腹痛、呕吐和偶尔发烧、脸色苍白、小而无法解释的瘀伤或口鼻出血、疲劳和易怒,意识模糊或癫痫发作、高血压和/或面部、手、脚或整个身体肿胀。免疫治疗引起的再生障碍性贫血可能包括疲劳、呼吸急促、心率加快或不规则、脸色苍白、不明原因或容易瘀伤、出血、皮疹、头晕、头痛和发烧。
ICPi 治疗引起的淋巴细胞减少可能表现为发烧、咳嗽、流鼻涕、淋巴结肿大、关节疼痛、皮疹和/或盗汗。免疫治疗引起的 ITP 可能表现为容易或过度的瘀伤、瘀点(通常在小腿上)、牙龈或鼻子出血以及尿液或粪便中的血液。获得性血友病 A 可表现为皮下出血和/或肌肉、胃肠道、泌尿生殖道和腹膜后出血。
一项荟萃分析报告了所有级别和 3~5 级贫血的汇总发生率分别为 9.8% 和 5%。大多数患者在ICPi治疗后出现反应,并通过皮质类固醇、静脉注射免疫球蛋白(IVIG)和生长因子获得缓解。溶血性贫血通常可以通过停用 ICPi、皮质类固醇和 IVIG 来治疗。
血小板减少症也相对少见。所有级别血小板减少症的合并发生率为 2.8%, 3~5 级发生率为1.8%。必须对血小板减少症的原因进行评估,包括评估 TTP、弥散性血管内凝血、骨髓增生异常综合征以及与 ICPi 相关的免疫介导的血小板减少症。皮质类固醇已被证明有效。
凝血因子相关的获得性出血障碍称之为获得性凝血因子Ⅷ缺乏症。在低滴度水平时,简单的因子替代和皮质类固醇可能有效;然而,在高滴度水平时(> 5 Bethesda),可能需要旁路试剂。
免疫相关心血管毒性
免疫相关心血管毒性可包括心肌炎、心包炎、心律失常、心室功能受损伴心力衰竭、血管炎和静脉血栓栓塞。发生心血管毒性的中位时间为 6 周。出现的症状可能包括进行性疲劳、肌痛或虚弱、心悸、胸痛、晕厥前兆或晕厥、气短和外周水肿。严重病例可出现心源性休克或猝死。
免疫治疗引起的血管炎和静脉血栓栓塞症(VTE)相关的症状可能包括疼痛、四肢肿胀、皮肤静脉可见度增加或紫癜、红斑和紫绀,伴有不明原因的发热、呼吸困难、胸痛、咳嗽、喘息或咯血。ICPi 相关心血管毒性很少见,但通常会导致严重后果,死亡率很高,患者常因顽固性心律失常或心源性休克死亡。
免疫介导的心肌炎可能导致心力衰竭和/或心律失常。心肌炎可能是暴发性、进行性甚至危及生命。急性心力衰竭可能继发于心脏功能下降和射血分数降低。传导异常可包括完全性心脏传导阻滞。可能会发生各种心律失常,包括可控的室上性心动过速或危及生命的室性心动过速。
出现症状时,超声心动图可能显示左心室或右心室射血分数降低(伴有整体或局部异常)。心脏 MRI 可以显示心肌炎的证据,但不如心内膜心肌活检敏感。对于不稳定或对初始治疗无效或诊断有疑问的患者,应考虑进行心内膜心肌活检。然而,当临床高度怀疑时,应在获得确诊病理学检查之前经验性地提供治疗。
小型回顾性系列研究发现,在接受免疫疗法治疗后,VTE 的发生率升高,据报道为 8%~30%。因此,管理重点在于治疗 VTE 和预防并发症(如肺栓塞)、避免免疫抑制治疗,以及当患者稳定时,在没有其他 irAE 的情况下可以继续应用ICPi。ICPi 引起的血管炎已被报道为大血管血管炎以及 PNS 和 CNS 血管炎,在停止治疗和/或皮质类固醇后可消退。
免疫相关眼部毒性
免疫相关眼部毒性包括葡萄膜炎、虹膜炎和巩膜外层炎。中位发病时间为 5 周。免疫治疗引起的眼部毒性相关的症状可能包括视力模糊、色觉改变、畏光、扭曲、暗点、视野改变、复视、触痛、眼球运动疼痛、眼睑肿胀、眼球突出、发红和/或干燥。与其他免疫相关毒性相比,眼部毒性不常见,其管理也不复杂。眼部毒性的主要机制是炎症,并且通常可以安全地继续使用 ICPi,大多数为轻度并且可以通过局部皮质类固醇进行控制。
表层巩膜炎是一种罕见但具有临床意义的免疫相关不良事件,发生率约< 1%。对于所有巩膜外层炎病例,建议转诊眼科,即使没有症状并且在评估完成之前一直保持免疫检查点抑制剂治疗。通常使用人工泪液、局部皮质类固醇和睫状肌麻痹剂治疗,极少数情况下需要全身性类固醇。任何视力受损(视力 < 20/40)都应紧急转诊眼科以评估是否需要更具体的干预措施。如果出现复发事件或 4 级表现(视力 20/200 或更差),建议永久停用 ICPi。英夫利昔单抗可用于严重和难治性病例,尽管仅基于病例报告。
免疫相关输液反应
免疫相关输液反应(IRR)并不常见,相关的症状通常表现为低烧、寒战、头痛或恶心。严重者可能出现心动过速、血压不稳定、低氧血症、胸痛、咳嗽、呼吸急促、喘息、潮红、出汗、荨麻疹或瘙痒、血管性水肿和先兆晕厥或晕厥等其他症状。
轻度IRR不需要干预,症状通常可以很快缓解。对于中度 IRR,再次激发时中断输注和减慢输注速度可能有效。可能需要给予支持疗法,即静脉输液、苯海拉明、对乙酰氨基酚、非甾体抗炎药或其他镇痛药。对于严重反应患者,建议根据机构指南停止治疗、静脉注射皮质类固醇和紧急干预。根据 IRR 的严重程度,使用苯海拉明和对乙酰氨基酚的预先给药可能会预防IRR。
类固醇应用相关的不良反应
类固醇仍然是免疫治疗相关 AE 管理中研究最多和最有价值的药物。类固醇的剂量提高和使用时间延长可能使患者面临发生急性和长期类固醇相关毒性的风险升高。评估患者的既往状况并仔细监测类固醇相关并发症至关重要。
对于需要长期使用类固醇的患者来说,给予预防某些机会性感染以及减轻各种毒性的措施是必要的。应在尽可能短的时间内尽量使用小剂量的类固醇,以减少类固醇的有害影响。某些患有糖尿病或免疫功能低下等疾病的患者和老年人需要特别关注。根据类固醇治疗irAE的情况和患者的耐受能力,类固醇应个体化的逐渐减量。多学科团队可用于管理某些类固醇相关并发症,决策时应参考指南。 (编译 余勇)














