残留浸润性疾病的HER2阳性乳腺癌 恩美曲妥珠单抗可改善患者总生存
美国匹兹堡大学医疗中心希尔曼癌症中心Geyer等报告,与曲妥珠单抗相比,恩美曲妥珠单抗(T-DM1)改善了新辅助治疗后伴有残留浸润性疾病的、人表皮生长因子受体2(HER2)阳性的、早期乳腺癌患者的总生存,并持续改善了无浸润性疾病生存。(N Engl J Med. 2025年1月15日在线版)
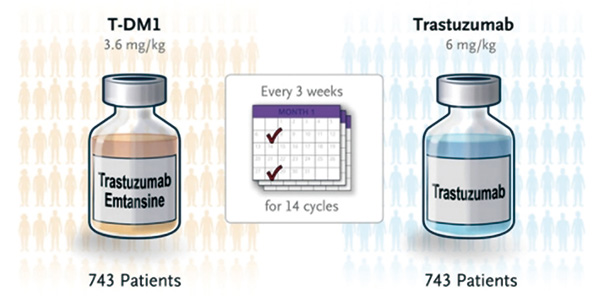
HER2阳性的早期乳腺癌患者在新辅助全身治疗后伴有残余浸润性疾病,其复发和死亡的风险很高。T-DM1(trastuzumab emtansine)是一种靶向HER2的抗体-药物偶联物(ADC),是曲妥珠单抗和美坦新的偶联物,让曲妥珠单抗与癌细胞上的HER2受体结合时,美坦新顺利进入癌细胞内部并杀死癌细胞。T-DM1在早期及晚期乳腺癌的应用均得到临床指南的推荐,是全球首个获批上市的乳腺癌ADC。
Ⅲ期开放标签试验KATHERINE的初步分析显示,在新辅助治疗后存在残留病灶的HER2阳性早期乳腺癌患者中,相比于标准辅助治疗,T-DM1辅助治疗可显著提高患者的3年无侵袭性疾病生存率(88.3% vs. 77.0%,HR=0.5,P<0.0001)。
该研究入组1486例紫杉烷为基础的化疗和曲妥珠单抗新辅助全身治疗后乳房或腋窝残留浸润性疾病的HER2阳性早期乳腺癌患者,患者均接受了至少6个周期的新辅助化疗,包括至少9周的紫杉烷化疗联合曲妥珠单抗治疗,新辅助治疗后存在残留病灶。手术后,将患者以1∶1的比例随机分配接受曲妥珠单抗标准辅助治疗(6 mg/kg,静脉注射,每3周一次)或T-DM1(3.6 mg/kg,静脉注射,每3周一次),共14个周期。在此报告了预先指定的无浸润性疾病生存的最终分析以及总生存的第二次中期分析。
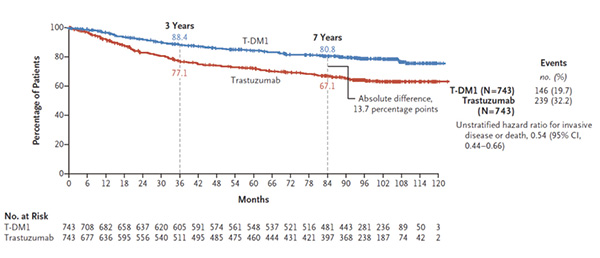
T-DM1组和标准辅助治疗组中位随访时间分别为101.4个月(8.45年)和100.8个月(8.4个月)。截至2023年10月5日,T-DM1组和标准辅助治疗组分别有70.1%(521例)和62.0%(461例)的患者生存且留在试验中,12%(89例)和17%(126例)患者死亡。
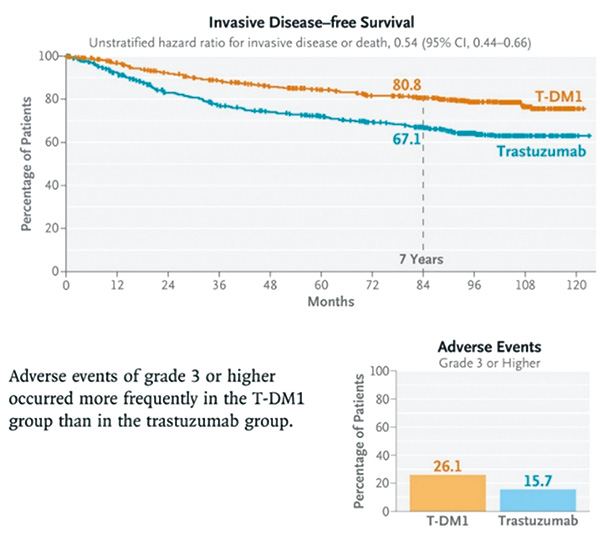
中位随访8.4年,与曲妥珠单抗标准辅助治疗相比,T-DM1持续改善了无浸润性疾病生存(浸润性疾病或死亡的未分层风险比为0.54,95%CI 0.44~0.66),侵袭性疾病或死亡长期风险降低了46%。T-DM1组的7年无浸润性疾病率为80.8%,曲妥珠单抗组为67.1%(差异为13.7%)。T-DM1导致的死亡风险也显著低于标准辅助治疗(未分层风险比为0.66,95%CI 0.51~0.87,P=0.003)。T-DM1组的7年总生存率为89.1%,标准辅助治疗组为84.4%(差异为4.7%),死亡风险降低34%(HR=0.66,95%CI 0.51~0.87,P=0.0003)。
亚组分析显示,无论激素受体状态、新辅助治疗方案、手术时病理淋巴结状态、年龄、种族、疾病严重程度等情况如何,T-DM1组的优势始终存在,发生侵袭性疾病事件或死亡事件风险整体降低约50%。
安全性方面,本次数据截止时与首次数据截止时(2018年7月25日)所报告的不良事件发生率和严重情况均类似。整个试验期间,T-DM1组和标准辅助治疗组分别有26.1%(193例)和15.7%(113例)患者发生3级或以上不良事件;分别有12.7%(94例)和8.1%(58例)患者发生严重不良事件。
研究解读
相比于2019年公布的数据,此次报告的研究结果显示T-DM1持续改善了iDFS,且OS也显著改善,且未发现新的安全性信号。该研究的长期随访数据证实了T-DM1是新辅助治疗后存在残留病灶的HER2阳性早期乳腺癌患者的有效辅助治疗方案。
研究者认为,该研究是一项具有里程碑意义的临床试验,研究发现了T-DM1具有很高的抗肿瘤活性,研究结果的报告时间比最终预设的时间要更早。该研究结果也改变了全球HER2阳性早期乳腺癌患者的标准治疗策略。
研究者团队还在探索另一款靶向HER2的ADC药物——德曲妥珠单抗(trastuzumab deruxtecan)用于其他类型乳腺癌患者如HER2低表达乳腺癌患者中的效果,这部分患者应用其他HER2靶向药物的治疗效果不如HER2高表达患者。
(编译 孙翔宇)