mRNA新抗原疫苗可长效抗击胰腺癌
美国纪念斯隆-凯特琳癌症中心Balachandran等报告的Ⅰ期临床试验显示,mRNA新抗原疫苗autogene cevumeran(BNT122)可持续降低手术切除胰腺导管腺癌(PDAC)患者疾病复发风险,对疫苗应答患者复发风险较未应答患者降低86%。(Nature. 2025年2月19日在线版)
胰腺癌致死率高被称为癌症之王,确诊患者5年生存率仅1%。即使确诊较早接受手术切除,约60%~80%患者术后会出现复发。mRNA疫苗在肿瘤治疗领域研究近年来取得进展,2023年mRNA疫苗荣获诺奖的前几个月,抗癌mRNA疫苗取得突破性进展。在治疗胰腺癌的Ⅰ期临床研究中,由基因泰克和BioNTech公司共同开发的mRNA个体化新抗原疫苗autogene cevumeran(BNT122)表现出良好的安全性和出色的疗效,50%的患者对疫苗治疗产生应答,且mRNA疫苗与化疗和免疫治疗的序贯联用,使胰腺癌的复发和患者死亡风险,较未实现应答的患者下降92%(HR=0.08)。
时隔两年,研究团队再次在《自然》杂志报告了这项试验的后续分析结果。结果表明,在接受手术切除肿瘤的PDAC患者中,这款个体化定制的mRNA新抗原疫苗可诱导患者产生肿瘤特异性的CD8阳性T细胞免疫应答,持续降低患者的疾病复发风险,改善患者生存。这些T细胞能够在患者体内维持效应功能长达3年以上,部分T细胞甚至寿命超过10年,提供长期免疫保护。
新抗原是指由肿瘤特异性基因突变产生的特异性蛋白质片段,仅由肿瘤细胞表达。这些突变蛋白被人体免疫系统识别为外来物,对其产生免疫反应。但PDAC往往无法产生高质量的新抗原,导致T细胞无法有效抗击。个体化疫苗开发处理是肿瘤特异性表达的新抗原,利用新抗原激活T细胞促进其增殖和迁移,从而发挥抗击肿瘤的作用。该研究中的mRNA新抗原疫苗可在一个mRNA分子中编码数十种新抗原,激发人体针对肿瘤细胞产生更全面的免疫反应,防止肿瘤细胞逃避免疫系统攻击。
这项Ⅰ期临床试验共招募16例PDAC患者,旨在初步评估mRNA新抗原疫苗autogene cevumeran的可行性和安全性。患者在根治性手术后接受单剂量PD-L1抑制剂阿替利珠单抗治疗,根据其肿瘤样本制备mRNA疫苗;患者接受8剂autogene cevumeran注射后,再行12个周期mFOLFIRINOX方案辅助化疗,最后注射1剂加强针疫苗。
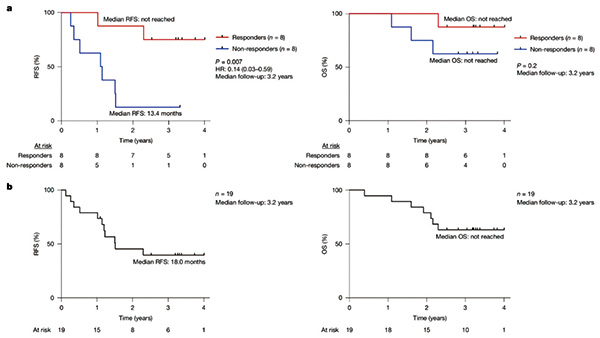
此次报告的结果显示,平均3.2年随访期内,8例患者在接种疫苗后产生了强烈的新抗原特异性CD8+T细胞免疫应答,且未出现肿瘤复发或死亡;其余8例对治疗无应答患者,中位无复发生存时间(RFS)为13.4个月(HR=0.14,95%CI 0.03~0.59,P=0.007)。
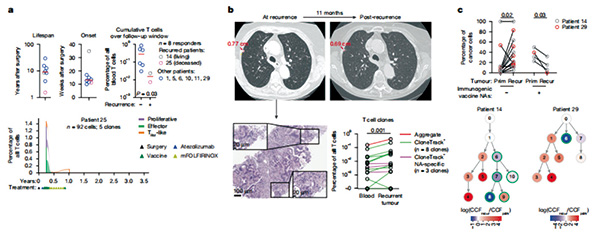
研究者使用CloneTrack技术,追踪了8例应答者的T细胞克隆动态变化。结果显示,疫苗诱导产生了29种针对新抗原有特异性反应的T细胞克隆。这些T细胞在疫苗初始接种后经历了显著扩增,约有77%在6次或更少的初始接种剂量后达到扩增峰值,扩增倍数可达100倍或更多。
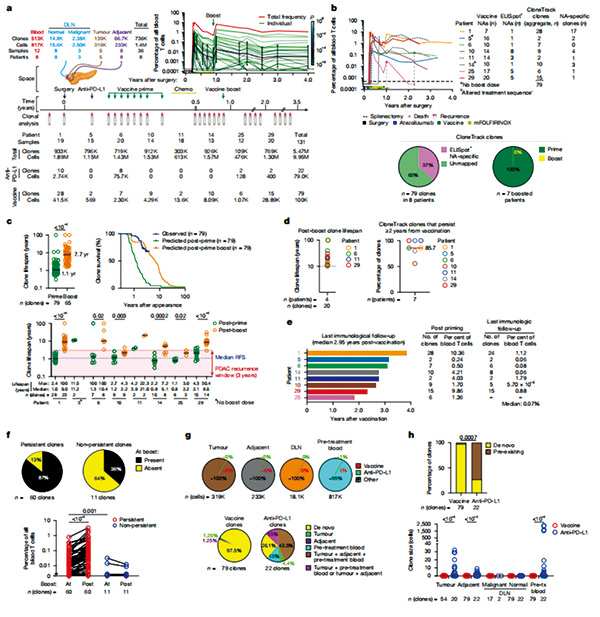
研究者发现,疫苗可激发持久的T细胞扩增,即使患者接受了可能损伤免疫系统的化疗,经疫苗诱导扩增的T细胞仍保持功能,且在接种疫苗加强针后能再次扩增。疫苗诱导产生的T细胞中位存活期为1.1年,半衰期约为40天。在接种加强针之后,这些T细胞的存活期更是显著延长,预计能达到7.7年,30%的T细胞克隆预估寿命甚至超过10年。这些靶向肿瘤新抗原的T细胞在血液循环中持久存在,有望发挥长久预防肿瘤复发的作用。
在接种疫苗后的2年多时间里(中位随访2.95年),研究者观察到86%的T细胞克隆仍然在患者的外周血中持续存活,占外周T细胞总数的0.07%左右,占比在接种疫苗3.8年后达到1.1%。
据悉,BioNTech已启动多项Ⅱ期临床试验,在结直肠癌、PDAC和黑色素瘤患者中评估autogene cevumeran作为辅助疗法的效果。
除了存活的时间长,这些T细胞还长期保持功能,不发生耗竭。从细胞表型来看,疫苗诱导产生的T细胞经历了从增殖状态到效应状态,再到组织驻留记忆T细胞样(TRM-like)状态的转变,并在TRM-like状态下保留较高的新抗原特异性效应功能。体外实验结果表明,在接种疫苗3.6年后,应答者的CD8+T细胞仍然能够有效识别和攻击新抗原,产生细胞因子IFN-γ、TNF-α并发挥细胞毒性作用。
应答者中,有2例患者肿瘤复发。研究者发现,复发的2例患者由疫苗诱导的新抗原特异性T细胞免疫反应较弱,且寿命短或免疫反应出现的时间晚。疫苗诱导产生的T细胞能浸润到患者的复发病灶,且携带疫苗新抗原的肿瘤细胞数量减少,表明疫苗的免疫反应对肿瘤细胞的突变产生了选择性压力。
该研究结果为mRNA疫苗作为肿瘤辅助治疗提供了强有力的支持,尤其是在针对肿瘤突变新抗原的个体化治疗方面。虽然尚需要更多的临床试验来确证这些结果,但这一发现为未来抗癌mRNA疫苗的广泛应用奠定了基础。
(编译 王悦宁)