HR+/HER2-转移性乳腺癌 PF-06873600有初步临床活性
美国MD安德森癌症中心Yap等报告的一项Ⅰ/Ⅱa期研究显示,PF-06873600的获益-风险特征与CDK4/6抑制剂类药物研究结果一致,在HR+/HER2-转移性乳腺癌中具有初步临床活性。(Clin Cancer Res. 2025年4月17日在线版)
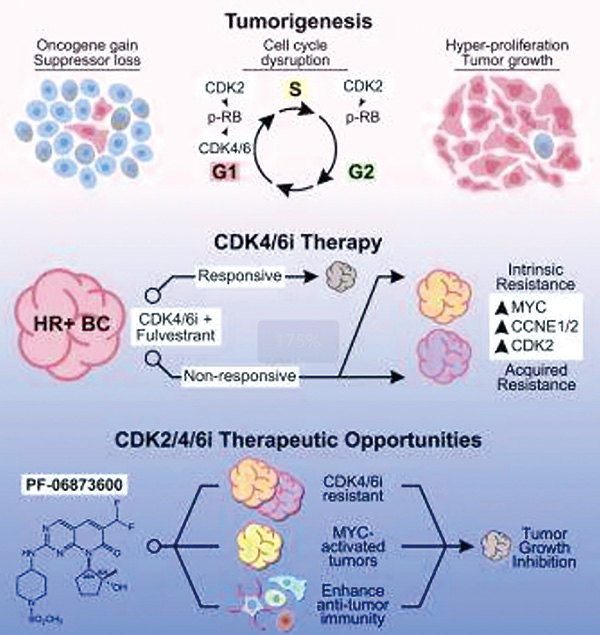
cyclin E过表达是一个关键的CDK4/6抑制剂耐药机制,这一发现重新激发了靶向CDK2的兴趣,同时抑制CDK2/4/6作为一种新的治疗方法。这项首次在人体中开展的研究评估了首创新药CDK2/4/6抑制剂PF-06873600的安全性、耐受性、药代动力学、药效学和疗效。
剂量递增队列纳入78例晚期乳腺癌、三阴性乳腺癌或卵巢癌患者,这些患者接受口服PF-06873600 1~50 mg bid(1A部分,51例),或PF-06873600联合内分泌治疗(1B部分,16例;1C部分11例)来确定推荐的扩展队列剂量(RDE)。剂量扩展队列(2A部分,45例;2C部分,28例)评估了RDE联合氟维司群治疗HR+/HER2-转移性乳腺癌患者时的初步抗肿瘤活性、安全性和耐受性。通过肿瘤活检和循环肿瘤DNA(ctDNA)中的磷酸化Rb和Ki67来评估药效学和转化读数。
PF-06873600的RDE为25 mg bid。在剂量递增期间,42例可评估患者中有6例(14.3%)出现与治疗相关的剂量限制性毒性。最常见的全因不良事件(151例)是恶心(62.9%)、贫血(44.4%)和疲劳(43.7%)。研究还观察到Ki67阳性细胞、pRb H-评分和ctDNA水平降低。在第1部分中观察到3例符合RECIST标准的部分缓解(PR)。在2A部分,有3例PR(客观缓解率ORR为6.7%,95%CI 1.4%~18.3%),在2C部分,有5例PR(ORR为22.7%,95%CI 7.8%~45.4%)。
(编译 周芸)


