DESTINY-Breast01研究 经治HER2阳性晚期乳腺癌 Trastuzumab deruxtecan单药ORR达60.9%
会上,Ian E Krop报告了DESTINY-Breast01研究,研究结果同步在线发表于《新英格兰医学杂志》。抗体药物偶联物Trastuzumab deruxtecan(DS-8201)显示持久的抗肿瘤活性,单药ORR达60.9%。
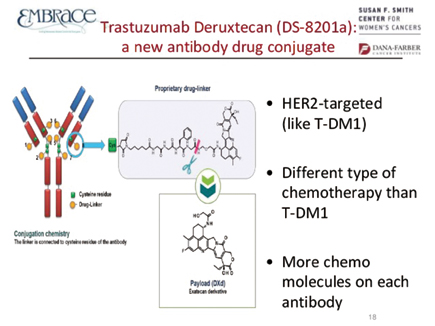
15%~20%的转移性乳腺癌患者HER2过表达或扩增,曲妥珠单抗+帕妥珠单抗+紫杉类为一线治疗方案,二线标准治疗为抗体药物偶联物T-DM1,目前没有公认的三线标准治疗,可用治疗方案的疗效有限,应答率为9%~ 31%,PFS为3~6个月。
Trastuzumab deruxtecan(DS-8201)是一种抗体药物偶联物,由一种靶向HER2的人源化单克隆抗体(与曲妥珠单抗有相同的氨基酸序列)、一种可切割的四肽连接物和一种有效的拓扑异构酶Ⅰ抑制剂组成。
DESTINY-Breast01是一项开放标签、单组、多中心的Ⅱ临床研究,旨在评估Trastuzumab deruxtecan在经T-DM1治疗后经病理学确认的HER2阳性转移性乳腺癌成人患者中的疗效和安全性。在第一部分中,研究者评估了三种不同剂量的疗效以确定推荐剂量;研究的第二部分旨在评估推荐剂量的有效性和安全性。主要的终点是独立评审委员会评估的ORR。关键次要终点包括疾病控制率、临床获益率、持续缓解时间和PFS和安全性。
2017年10月至2018年9月,共纳入北美、亚洲和欧洲8个国家253例患者,184例患者接受了推荐剂量5.4mg/kg,截止日期为2019年8月。接受推荐剂量患者的中位年龄为55岁,23.9%患者为65岁以上。在184例患者中,有97例(52.7%)患者为激素受体阳性,接受之前治疗的中位线数为6,包括T-DM1(100%)、曲妥珠单抗(100%)、帕妥珠单抗(65.8%)、其他HER2治疗(54.3%)。
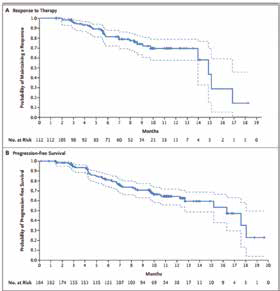
在184例接受推荐剂量(5.4mg/kg)的患者中,独立评审委员会评估的ORR为60.9%,其中,6.0%患者完全缓解,54.9%患者达到部分缓解,大部分患者的肿瘤大小相比基线时有缩小。疾病控制率为97.3%,临床获益率为76.1%,中位至缓解时间为1.6个月,与基线后第一次成像时间相对应。

亚组分析显示了一致的缓解情况,之前接受帕妥珠单抗患者、激素受体阳性患者、阴性患者、接受T-DM1治疗后先接受的Trastuzumab deruxtecan的ORR分别为64%、58%、66%和64%。
中位缓解持续时间为14.8个月,所有患者和无症状脑转移(24例)患者的中位PFS分别为16.4个月和18.1个月,预计6个月和12个月的预计生存率为93.9%和86.2%,中位OS尚未达到。
最常见的3级或以上不良事件是中性粒细胞计数下降(20.7%)、贫血(8.7%)和恶心(7.6%),研究期间,可能有13.6%的患者与间质性肺病相关(1级或2级,10.9%;3级或4级,0.5%;5级,2.2%)。
Trastuzumab deruxtecan在经治HER2阳性转移性乳腺癌患者中显示了持久的抗肿瘤活性。除了恶心和骨髓抑制外,在亚组患者中观察到间质性肺疾病,需注意肺部症状并仔细监测。
(编译 张娜)


